Una guía sobre probióticos y salud1
La Organización Mundial de la Salud (OMS) define los probióticos como "microorganismos vivos que, cuando se administran en cantidades adecuadas, confieren beneficios para la salud del huésped" (Hill et al. 2014) . En los Estados Unidos, los probióticos se consideran suplementos dietéticos, no alimentos o drogas, y por lo tanto no están específicamente regulados por la Administración de Alimentos y Medicamentos (FDA). Como suplementos dietéticos, algunos productos que contienen microorganismos vivos se han comercializado como probióticos sin haber sido sometidos a pruebas necesarias para confirmar sus beneficios para la salud. Se recomienda que sólo se consideren probióticos a las especies microbianas que han demostrado conferir beneficios para la salud en estudios bien diseñados y controlados (Hill et al. 2014). Los cultivos vivos usados ??en la fermentación de alimentos (por ejemplo, yogur) y que no tienen demostrados beneficios para la salud, no se consideran probióticos.
Los probióticos son beneficiosos para el bienestar gastrointestinal, inmunidad y una variedad de otros efectos en la salud (Sánchez et al. 2016). Hay muchos suplementos probióticos disponibles en el mercado y la elección de uno de ellos puede ser un reto. Esta revisión proporciona un resumen de los beneficios para la salud de probióticos que están respaldados por un alto nivel de evidencia científica.
Muchas bacterias y otros microorganismos han sido probados por sus efectos beneficiosos sobre la salud. Es importante tener en cuenta que estos microorganismos pueden diferir en sus efectos sobre la salud, por lo que cada probiótico potencial necesita ser probado para determinar si ejerce un beneficio específico en la salud. La investigación llevada a cabo en animales por sí sola no puede utilizarse para apoyar las recomendaciones para los seres humanos. Los trabajos de investigación en seres humanos deben completarse en todos los potenciales probióticos. Además, un efecto positivo en la salud a partir de un único trabajo de investigación en humano no es suficiente para confirmar los beneficios para la salud de un probiótico. Numerosos estudios bien diseñados que demuestren resultados positivos similares proporcionan la prueba más fuerte que un probiótico es eficiente.
Un alto nivel de evidencia científica es considerado una revisión sistemática con metaanálisis. Una revisión sistemática es una búsqueda y revisión estructurada de todos los estudios hasta la fecha, examinando un beneficio específico de los probióticos para la salud. En la investigación en salud, es común agrupar y analizar estadísticamente los resultados de los estudios, una técnica conocida como metaanálisis. Los hallazgos positivos de una revisión sistemática con metaanálisis sugieren fuertemente la eficacia, es decir, el probiótico ejerce un beneficio específico en la salud. Se ha sugerido que revisiones sistemáticas deberían realizarse en estudios de una sola especie (McFarland 2016), aunque la mayoría de las revisiones hasta la fecha han combinado distintas especies. Muchos de los beneficios en la salud de probióticos descritos en esta revisión tienen este fuerte nivel de evidencia científica. Sin embargo, es importante señalar que hay muchas más cepas que pueden ser eficaces, pero aún no han sido estudiadas.
Probióticos y sus beneficios para la salud
Los probióticos difieren en sus efectos sobre la salud humana. La mayoría de los probióticos provienen de los géneros Bifidobacterium o Lactobacillus. Diversas especies de Bifidobacterium (B. adolescentis, B. animalis, B. bifidum, B. breve y B. longum) y Lactobacillus (L. acidophilus, L. casei, L. fermentum, L. gasseri, L. johnsonii, L. paracasei, L. plantarum, y L. rhamnosus) proporcionan beneficios generales para la salud (Health Canada 2009). La dosis del probiótico ingerido, medida en "unidades formadoras de colonias" o UFC, es importante para la efectividad. Se cree que se necesita una dosis mínima de 1 × 109 (1 billón) de UFC por porción para proporcionar beneficios generales para la salud (Health Canada 2009).
Los probióticos ejercen beneficios para la salud mediante una serie de mecanismos. La mayoría de los probióticos inhiben el crecimiento de patógenos y producen productos de fermentación beneficos como ácidos grasos de cadena corta (Hill et al. 2014; Oelschlaeger 2010). Muchas especies probióticas producen vitaminas y enzimas útiles que ayudan a mantener la salud intestinal. Algunas cepas probióticas tienen efectos sobre el sistema inmunológico, neurológico u otros, además algunas cepas probióticas son consideradas fármacos porque se ha demostrado que pueden prevenir o tratar enfermedades (McFarland, Evans, y Goldstein 2018).
Salud digestiva
Estreñimiento
Una condición gastrointestinal común es el estreñimiento. Aquellos que sufren de estreñimiento a menudo se quejan de heces duras (y poco frecuentes) que son difíciles de pasar. La falta de fibra dietética, condiciones médicas y ciertos medicamentos son causas comunes de estreñimiento.
Una de las principales funciones del colon es la eliminación del agua. Esto es importante para prevenir la diarrea. Sin embargo, cuanto más tiempo el material permanezca en el colon, más agua se eliminará. Si el tiempo gastado en el colon es extenso, el resultado sería estreñimiento. El tiempo de tránsito es el tiempo que toma el contenido del tracto gastrointestinal en moverse a través del cuerpo. La mayor parte de este tiempo se gasta en el colon. Cuando el tiempo de tránsito es lento, de muchos días, el resultado son heces duras que son difíciles de pasar. La forma de las heces o la clasificación de consistencia es un indicador útil del tiempo de tránsito (heces duras = tránsito lento; heces blandas = tránsito normal; heces líquidas = tránsito rápido).
Los probióticos son eficaces en acelerar el tiempo de tránsito en adultos y son más efectivos en personas con estreñimiento (Dimidi et al. 2014; Miller, Zimmermann, y Ouwehand 2016; Zhang et al. 2020). La consistencia de las heces responde a los cambios en el tiempo de tránsito y puede mejorar con ciertos probióticos. Una revisión sistemática respalda que los probióticos, específicamente los probióticos de múltiples cepas, mejoraron significativamente la consistencia de las heces (las heces se volvieron más blandas) y la frecuencia de las heces (Zhang et al. 2020). Por el contrario, una revisión previa, que incluye diferentes estudios, proporcionó algunas pruebas de que los probióticos de una sola cepa pueden ser más efectivos que los probióticos de varias cepas (Dimidi et al. 2014). También hay evidencia contradictoria sobre la efectividad de las cepas de Bifidobacterium lactis (B. lactis) en los resultados del estreñimiento (Zhang et al. 2020; Dimidi et al. 2014), y por lo tanto se necesita más investigación.
Diarrea
La diarrea se define comúnmente como heces frecuentes, sueltas o acuosas y es a menudo causada por patógenos. Potenciales probióticos han sido evaluados en distintos trabajos para determinar si son eficaces en la prevención de diversos tipos de diarrea en adultos, incluyendo diarrea asociada a antibióticos y/o inducida por quimioterapia. La diarrea por Clostridium difficile es la diarrea más comúnmente asociada a antibióticos.
La evidencia de una revisión sistemática y un metanálisis respalda que los probióticos reducen la incidencia de diarrea asociada a Clostridium difficile y otras diarreas asociadas a antibióticos, siendo Lactobacillus casei el más efectivo (Ma et al. 2020). Además, la duración de la diarrea y el tiempo hasta el inicio de la diarrea mejoraron con varios probióticos (Ma et al. 2020). Una revisión previa de ensayos que usaban Lactobacillus spp., Saccharomyces spp. y combinaciones de probióticos también mostró un riesgo reducido de diarrea (Lau y Chamberlain 2016). Sin embargo, un metaanálisis, que separó a los participantes por edad, encontró que la administración de probióticos no redujo el riesgo de diarrea asociada a antibióticos en adultos mayores de 65 años (Jafarnejad et al. 2016).
También se ha llevado a cabo un metaanálisis sobre cepas específicas de probióticos y su eficacia en diarrea asociada a antibióticos. Lactobacillus rhamnosus GG, Lactobacillus casei, Bacillus clausii, Saccharomyces boulardii, Lactobacillus acidophilus y Multi-genera II son más efectivos que el placebo para ayudar a prevenir la diarrea asociada a antibióticos (Cai et al. 2018). Lactobacillus rhamnosus GG es eficaz para disminuir el riesgo a diarrea asociada a antibióticos en niños, pero en adultos, sólo en aquellos que recibieron antibióticos para la erradicación de H. pylori (ver sección más adelante). Lactobacillus rhamnosusfue efectivo (Szajewska y Kolodziej 2015a). Saccharomyces boulardii es eficaz en adultos, pero no específicamente contra diarrea asociada a Clostridium difficile (Szajewska y Kolodziej 2015b).
Un metaanálisis ha demostrado que los probióticos evaluados hasta la fecha disminuyen la diarrea inducida por radioterapia, pero no aquella inducida por quimioterapia en pacientes con cáncer abdominal y pélvico (Wang et al. 2016). Sin embargo, un metaanálisis más reciente mostró que la aplicación de probióticos antes o durante la quimioterapia previno efectivamente la aparición de diarrea inducida por quimioterapia entre pacientes con cáncer (Lu et al. 2019).
Síndrome de intestino irritable (SII)
El Síndrome del Intestino Irritable (SII) es una condición del tracto intestinal que resulta en dolor abdominal y/o incomodidad con hábitos intestinales alterados (diarrea y/o estreñimiento).
Una revisión sistemática que utiliza los criterios de diagnóstico médico del SII (Roma III) mostró que los probióticos mejoraron los puntajes generales de los síntomas y la calidad de vida en individuos con SII (Zhang, Li et al. 2016). Las dosis de probióticos de <1010 UFC y los probióticos de una sola cepa pueden ser más efectivas que las formulaciones de varias cepas para el alivio de los síntomas. Específicamente, Lactobacillus acidophilus-SDC, Lactobacillus plantarum 299v, Bacillus coagulans y Bifidobacterium bifidum MIMBb75 mejoraron las puntuaciones generales de síntomas en pacientes con SII, y Bifidobacterium bifidum MIMBb7 mejoró la calidad de vida. Una revisión sistemática más reciente y un metaanálisis de estudios que utilizan Roma I, II o III para diagnosticar a individuos con SII descubrieron que los probióticos mejoraron significativamente los síntomas generales del SII (Asha y Khalil 2020). Sin embargo, el metaanálisis no mostró diferencias en las puntuaciones de dolor abdominal con los probióticos en general en comparación con los placebos, pero las puntuaciones de dolor abdominal se redujeron con los probióticos que contienen Lactobacillus spp.
Infección por H. pylori y enfermedad de la úlcera péptica
La infección con Helicobacter pylori (H. pylori), patógeno bacteriano, causa gastritis (inflamación del revestimiento del estómago) y, si no se trata, puede conducir a úlceras gástricas y cáncer. El tratamiento recomendado actualmente para H. pylori es una combinación de antibióticos con un inhibidor de la bomba de protones (medicamento para reducir el ácido del estómago) (Li et al. 2015). Sin embargo, el tratamiento puede causar náuseas, vómitos y diarrea.
Se ha evaluado la eficacia de varias mezclas de probióticos para mejorar el tratamiento (tasas de erradicación) de la infección por H. pylori y prevenir los efectos secundarios del tratamiento (Lu, Yu et al. 2016; McFarland et al. 2016; Lv et al. 2015; Zhang et al. 2015; Gong, Li y Sun 2015). En un metaanálisis que examinó 40 ensayos controlados, los probióticos mejoraron la tasa de erradicación y disminuyeron los efectos secundarios cuando se agregaron a los tratamientos con antibióticos diseñados para erradicar H. pylori, especialmente cuando se usaron antes y durante el tratamiento de erradicación y durante más de 2 semanas (Shi et al. 2019). En comparación con un grupo de control, Lactobacillus spp., Saccharomyces spp. y múltiples cepas demostraron mejoras significativas en las tasas de erradicación. Otras cepas pueden ser efectivas, pero se necesita más investigación.
Enfermedad diverticular
La enfermedad diverticular es una enfermedad gastrointestinal común, especialmente en adultos mayores. Muchos adultos mayores tienen diverticulosis (divertículos colónicos, es decir, desprendimiento del colon) pero no presentan síntomas. Otros desarrollan síntomas como dolor abdominal, malestar y cambios en el hábito intestinal. Una minoría de individuos con diverticulosis desarrollan diverticulitis, una inflamación aguda de los divertículos.
Hubo muy pocos estudios de calidad que evalúen el efecto de probióticos en la enfermedad diverticular (Lahner et al. 2016). Los probióticos pueden ser potencialmente beneficiosos en el manejo de los síntomas de la enfermedad; sin embargo, se necesita más investigación antes de poder hacer recomendaciones.
Metabolismo
Peso corporal
Aunque los probióticos están asociados más frecuentemente con la salud gastrointestinal, también pueden tener efectos sistémicos, incluyendo la influencia sobre el peso corporal. En una revisión reciente con metaanálisis, los probióticos de cepas múltiples y cepas simples redujeron el peso corporal, el índice de masa corporal, la circunferencia de la cintura, la masa de grasa y el porcentaje de grasa (Wang et al. 2019). Los efectos fueron más fuertes con altas dosis y probióticos de una sola cepa. Hallazgos similares fueron confirmados por una segunda revisión (Koutnikova et al. 2019). Actualmente, no se pueden hacer recomendaciones específicas con respecto a la mejor combinación de cepas y dosis para la reducción de peso corporal.
Diabetes tipo 2
El objetivo del exitoso manejo de la diabetes tipo 2 es lograr que la glucosa y la hemoglobina A1c en sangre, prueba de sangre usada para estimar los niveles promedio de glucosa durante un período de tres meses, sean casi normales. En tres trabajos que evaluaron probióticos en participantes con diabetes tipo 2, la glucosa en ayunas fue menor con suplementos probióticos en comparación con el placebo (Samah et al. 2016; Zhang, Wu y Fei 2016; Li et al. 2016). Los trabajos difirieron en sus conclusiones con respecto a los probióticos y A1c, con un trabajo mostrando un descenso y el otro ningún efecto. Sin embargo, los estudios incluidos fueron de sólo cuatro a ocho semanas de duración, demasiado corto para esperar cambios en A1c. En una revisión más reciente de estudios y metaanálisis que evalúan el efecto de la ingesta oral de probióticos en variables relacionadas con la obesidad, la diabetes y la enfermedad del hígado graso no alcohólico, se descubrió que los probióticos reducen la glucosa en ayunas, la hemoglobina glucosilada y la insulina (Koutnikova et al. 2019). Estas mejoras se observaron con Bifidobacterium breve, Bifidobacterium longum, Streptococcus salivarius subsp. thermophilus, Lactobacillus acidophilus, Lactobacillus casei y Lactobacillus delbrueckii que contienen mezclas.
Colesterol
El colesterol sérico total elevado y el colesterol LDL (lipoproteína de baja densidad) son factores de riesgo de enfermedad cardiovascular. El consumo de probióticos resultó en disminuciones significativas en colesterol total y LDL (Cho y Kim 2015). Los probióticos no tuvieron efecto sobre el colesterol HDL (lipoproteína de alta densidad) ni sobre triglicéridos. Lactobacillus acidophilus solo y en combinación con L. lactis y L. plantarum mostraron efectos benéficos independientes. Al igual que con otros ensayos de colesterol, los participantes con más altos niveles de colesterol presentaron los mejores beneficios. Una revisión más reciente de estudios concluyó que la administración de probióticos resultó en reducciones significativas de colesterol total, colesterol LDL y triglicéridos y un aumento del colesterol HDL (Tenorio-Jiménez et al. 2020). Sin embargo, algunos de los estudios evaluados utilizaron los probióticos en combinación con otros compuestos, lo que hace que sea más difícil determinar los efectos específicos de los probióticos.
Infección
Infecciones del tracto urinario
Se evaluó el efecto de una variedad de cepas, formulaciones y dosis de probióticos para la prevención de infecciones del tracto urinario (Schwenger, Tejani, y Loewen 2015). No se observaron beneficios, pero la mayoría de los estudios eran pequeños y de mala calidad. Es necesario mayor investigación para determinar si existe una relación entre el consumo de probióticos e infecciones del tracto urinario.
Infecciones respiratorias
Las infecciones del tracto respiratorio superior (URTI por sus siglas en inglés), como el resfriado común, a menudo se deben a virus. Durante varios años, las pruebas de metaanálisis han apoyado el papel de la ingesta oral de probióticos y potenciales probióticos para la disminución de la incidencia de URTI aguda, la duración de la URTI y el uso de antibióticos relacionados (Hao, Dong y Wu 2015). Sin embargo, se necesitan estudios confirmatorios de investigación de mejor calidad. Una revisión de los estudios y el metaanálisis con varias formulaciones de probióticos, incluidos los que contienen Lactobacillus y Bifidobacterium spp., encontró que los bebés y niños que recibieron probióticos para prevenir enfermedades agudas tenían un menor riesgo de recibir antibióticos recetados, en comparación con los que recibieron un placebo (King et al. 2018).
Enfermedad periodontal
Los probióticos pueden ser beneficiosos en la prevención y tratamiento de caries dentales y otras enfermedades periodontales. Sin embargo, una reciente revisión sistemática mostró que cuatro estudios encontraron beneficios de usar probióticos como terapia adyuvante en periodontitis crónica, mientras tres estudios encontraron ningún beneficio comparado con placebo (Ikriam et al. 2018). Probióticos, Bifidobacterium spp. en particular, han demostrado reducir la población de Streptococcus mutans, una bacteria ligada a las caries dentales y además puede ayudar a controlar gingivitis y periodontitis (Gruner, Paris y Schwendicke 2016).
Sugerencias de compras de probióticos
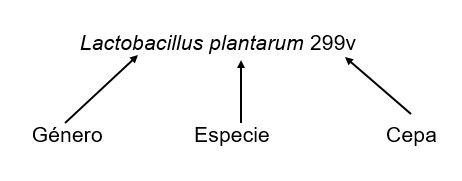
Aunque es necesario mayor investigación para determinar los efectos en salud de muchos potenciales probióticos, es aconsejable seleccionar uno que haya sido bien estudiado con demostrados beneficios para la salud. Al elegir un probiótico, asegúrese de que el mismo se describa por género, especie y cepa en la etiqueta (véase la figura 1 a continuación). Al tomar una decisión de compra, busque información sobre el género y la especie y el beneficio de salud que está buscando. Si el efecto sobre la salud es específico de la cepa, busque la información de la cepa (nombrada por género, especie y número de cepa). La etiqueta debe indicar claramente el número de células viables (UFC), que debe exceder, como mínimo, 1 × 109 (1 billón). Siga las recomendaciones del fabricante para su almacenamiento, debido que algunos probióticos requieren refrigeración, mientras que muchos otros se pueden almacenar a temperatura ambiente.
Referencias
Asha, M. Z., and S. F. H. Khalil. 2020. "Efficacy and Safety of Probiotics, Prebiotics and Synbiotics in the Treatment of Irritable Bowel Syndrome: A Systematic Review and Meta- Analysis." Sultan Qaboos University Medical Journal 20 (1): e13–e24. https://doi.org/10.18295/squmj.2020.20.01.003
Cho, Y. A., and J. Kim. 2015. "Effect of Probiotics on Blood Lipid Concentrations: A Meta-Analysis of Randomized Controlled Trials." Medicine (Baltimore) 94 (43): e1714. https://doi.org/10.1097/md.0000000000001714
Dimidi, E., S. Christodoulides, K. C. Fragko, S. M. Scott, and K. Whelan. 2014. "The Effect of Probiotics On Functional Constipation In Adults: A Systematic Review and Meta-Analysis of Randomized Controlled Trials." American Journal of Clinical Nutrition 100 (4): 1075–1084. https://doi.org/10.3945/ajcn.114.089151h
Food and Agricultural Organization of the United Nations and World Health Organization. 2002. Guidelines for the Evaluation of Probiotics in Food. Food and Agricultural Organization of the United Nations. https://www.foodinprogress.com/wp-content/uploads/2019/04/Guidelines-for-the-Evaluation-of-Probiotics-in-Food.pdf. Accessed February 14, 2023.
Goldenberg, J. Z., S. S. Ma, J. D. Saxton, M. R. Martzen, P. O. Vandvik, K. Thorlund, G. H. Guyatt, and B. C. Johnston. 2013. "Probiotics for the Prevention of Clostridium difficile-Associated Diarrhea in Adults and Children." The Cochrane Database of Systematic Review (5):Cd006095. https://doi.org/10.1002/14651858.CD006095.pub3
Gong, Y., Y. Li, and Q. Sun. 2015. "Probiotics Improve Efficacy and Tolerability of Triple Therapy to Eradicate Helicobacter Pylori: A Meta-Analysis of Randomized Controlled Trials." The International Journal of Clinical and Experimental Medicine 8 (4): 6530–43. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4483842/
Gruner, D., S. Paris, and F. Schwendicke. 2016. "Probiotics for Managing Caries and Periodontitis: Systematic Review and Meta-Analysis." Journal of Dentistry 48:16–25. https://doi.org/10.1016/j.jdent.2016.03.002
Hao, Q., B. R. Dong, and T. Wu. 2015. "Probiotics for Preventing Acute Upper Respiratory Tract Infections." The Cochrane Database of Systematic Review 2:Cd006895. https://doi.org/10.1002/14651858.CD006895.pub3
Health Canada. 2009. "Accepted Claims about the Nature of Probiotic Microorganisms in Food." Accessed March 30, 2020. http://hc-sc.gc.ca/fn-an/label-etiquet/claims-reclam/probiotics_claims-allegations_probiotiques-eng.php
Hill, C., F. Guarner, G. Reid, G. R. Gibson, D. J. Merenstein, B. Pot, L. Morelli, R. B. Canani, H. J. Flint, S. Salminen, P. C. Calder, and M. E. Sanders. 2014. "The International Scientific Association for Probiotics and Prebiotics Consensus Statement on The Scope and Appropriate Use of the Term Probiotic." Nature Reviews Gastroenterology & Hepatology 11 (8): 506–14. https://doi.org/10.1038/nrgastro.2014.66
Ikram, S., N. Hassan, M. A. Raffat, S. Mirza, and Z. Akram. 2018. "Systematic Review and Meta-Analysis of Double-Blind, Placebo-Controlled, Randomized Clinical Trials Using Probiotics in Chronic Periodontitis." Journal of Investigative and Clinical Dentistry 9 (3): e12338. https://doi.org/10.1111/jicd.12338
Jafarnejad, S., S. Shab-Bidar, J. R. Speakman, K. Parastui, M. Daneshi-Maskooni, and K. Djafarian. 2016. "Probiotics Reduce the Risk of Antibiotic-Associated Diarrhea in Adults (18–64 Years) but Not the Elderly (>65 Years): A Meta-Analysis." Nutrition in Clinical Practice 31 (4): 502–13. https://doi.org/10.1177/0884533616639399
King, S., D. Tancredi, I. Lenoir-Wijnkoop, K. Gould, H. Vann, G. Connors, M. E. Sanders, J. A. Linder, A. L. Shane, and D. Merenstein. 2018. "Does Probiotic Consumption Reduce Antibiotic Utilization for Common Acute Infections? A Systematic Review and Meta-Analysis." European Journal of Public Health 29 (3): 494–499. https://doi.org/10.1093/eurpub/cky185
Koutnikova, H., B. Genser, M. Monteiro-Sepulveda, J. M. Faurie, S. Rizkalla, J. Schrezenmeir, and K. Clément. 2019. "Impact of Bacterial Probiotics on Obesity, Diabetes and Non-Alcoholic Fatty Liver Disease Related Variables: A Systematic Review and Meta-Analysis of Randomised Con- trolled Trials." BMJ 9 (3): e017995. https://doi.org/10.1136/bmjopen-2017-017995
Lahner, E., C. Bellisario, C. Hassan, A. Zullo, G. Esposito, and B. Annibale. 2016. "Probiotics in the Treatment of Diverticular Disease. A Systematic Review." Journal of Gastrointestinal and Liver Diseases 25 (1): 79–86. https://doi.org/10.15403/jgld.2014.1121.251.srw
Lau, C. S., and R. S. Chamberlain. 2016. "Probiotics Are Effective at Preventing Clostridium difficile-Associated Diarrhea: A Systematic Review and Meta-Analysis." Inter- national Journal of General Medicine 9:27–37. https://doi.org/10.2147/ijgm.s98280
Li, B. Z., D. E. Threapleton, J. Y. Wang, J. M. Xu, J. Q. Yuan, C. Zhang, P. Li, Q. L. Ye, B. Guo, C. Mao, and D. Q. Ye. 2015. "Comparative Effectiveness and Tolerance of Treatments For Helicobacter Pylori: Systematic Review And Network Meta-Analysis." BMJ 351:h4052. https://doi.org/10.1136/bmj.h4052
Li, C., X. Li, H. Han, H. Cui, M. Peng, G. Wang, and Z. Wang. 2016. "Effect of Probiotics on Metabolic Profiles in Type 2 Diabetes Mellitus: A Meta-Analysis of Randomized, Controlled Trials." Medicine (Baltimore) 95 (26): e4088. https://doi.org/10.1097/md.0000000000004088
Lu, D., J. Yan, F. Liu, P. Ding, B. Chen, Y. Lu, and Z. Sun. 2019. "Probiotics in Preventing and Treating Chemotherapy-Induced Diarrhea: A Meta-Analysis." Asia Pacific Clinical Nutrition Society 28 (4): 701–710. https://doi.org/10.6133/apjcn.201912_28(4).0005
Lu, M., S. Yu, J. Deng, Q. Yan, C. Yang, G. Xia, and X. Zhou. 2016. "Efficacy of Probiotic Supplementation Therapy for Helicobacter pylori Eradication: A Meta-Analysis of Ran- domized Controlled Trials." PLoS One 11 (10): e0163743. https://doi.org/10.1371/journal.pone.0163743
Lv, Z., B. Wang, X. Zhou, F. Wang, Y. Xie, H. Zheng, and N. Lv. 2015. "Efficacy and Safety of Probiotics as Adjuvant Agents for Helicobacter pylori Infection: A Meta-Analysis." Experimental and Therapeutic Medicine 9 (3): 707–716. https://doi.org/10.3892/etm.2015.2174
Ma, Y., J. Y. Yang, X. Peng, K. Y. Xiao, Q. X., and C. Wang. 2020. "Which Probiotic Has the Best Effect on Preventing Clostridium difficile-Associated Diarrhea? A Systematic Review and Network Meta-Analysis." Journal of Digestive Diseases 21 (2): 69–80. https://doi. org/10.1111/1751-2980.12839
McFarland, L. V. 2016. "An Observation on Inappropriate Probiotic Subgroup Classifications in the Meta-Analysis by Lau and Chamberlain." International Journal of General Medicine 9:333–336. https://doi.org/10.2147/ijgm.s119970
McFarland, L. V., C. T. Evans, and E. J. Goldstein. 2018. "Strain-Specificity and Disease-Specificity of Probiotic Efficacy: A Systematic Review and Meta-Analysis." Frontiers in Medicine 5 (124). https://doi.org/10.3389/fmed.2018.00124
McFarland, L. V., Y. Huang, L. Wang, and P. Malfertheiner. 2016. "Systematic Review and Meta-Analysis: Multi-Strain Probiotics as Adjunct Therapy for Helicobacter pylori Eradication and Prevention of Adverse Events." United European Gastroenterology Journal 4 (4): 546–61. https:// doi.org/10.1177/2050640615617358
McFarland, L. V., P. Malfertheiner, Y. Huang, and L. Wang. 2015. "Meta-Analysis of Single Strain Probiotics for the Eradication of Helicobacter pylori and Prevention of Ad- verse Events." World Journal of Meta-Analysis 3 (2): 97–117. https://doi.org/10.13105/wjma.v3.i2.97
Miller, L. E., A. K. Zimmermann, and A. C. Ouwehand. 2016. "Contemporary Meta-Analysis of Short-Term Probiotic Consumption on Gastrointestinal Transit." World Journal of Gastroenterology 22 (21): 5122–31. https://doi. org/10.3748/wjg.v22.i21.5122
Oelschlaeger, T. A. 2010. "Mechanisms of Probiotic Actions—A Review." International Journal of Medical Microbiology i 300 (1): 57–62. https://doi.org/10.1016/j.ijmm.2009.08.005
Pattani, R., V. A. Palda, S. W. Hwang, and P. S. Shah. 2013. "Probiotics for the Prevention of Antibiotic-Associated Diarrhea and Clostridium difficile Infection among Hos- pitalized Patients: Systematic Review and Meta-Analysis." Open Medicine 7 (2): e56–67. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3863752/
Samah, S., K. Ramasamy, S. M. Lim, and C. F. Neoh. 2016. "Probiotics for the Management of Type 2 Diabetes Mel- litus: A Systematic Review and Meta-Analysis." Diabetes Research and Clinical Practice 118:172–182. https://doi. org/10.1016/j.diabres.2016.06.014
Sanchez, B., S. Delgado, A. Blanco-Miguez, A. Lourenco, M. Gueimonde, and A. Margolles. 2016. "Probiotics, Gut Microbiota and Their Influence on Host Health and Disease." Molecular Nutrition and Food Research 61 (1): 1600240. https://doi.org/10.1002/mnfr.201600240
Schwenger, E. M., A. M. Tejani, and P. S. Loewen. 2015. "Probiotics for Preventing Urinary Tract Infections in Adults and Children." Cochrane Database of Systematic Review (12):Cd008772. https://doi.org/10.1002/14651858.CD008772.pub2
Shi, X., J. Zhang, L. Mo, J. Shi, M. Qin, and X. Huang. 2019. "Efficacy and Safety of Probiotics in Eradicating Helicobacter pylori: A Network Meta-Analysis." Medicine 98 (15): e15180–e15180. https://doi.org/10.1097/MD.0000000000015180
Szajewska, H., and M. Kolodziej. 2015a. "Systematic Review with Meta-Analysis: Lactobacillus rhamnosus GG in the Prevention of Antibiotic-Associated Diarrhoea in Children and Adults." Alimentary Pharmacology & Therapeutics 42 (10): 1149–57. https://doi.org/10.1111/apt.13404
Szajewska, H., and M. Kolodziej. 2015b. "Systematic Review with Meta-Analysis: Saccharomyces boulardii in the Prevention of Antibiotic-Associated Diarrhoea." Alimentary Pharmacology & Therapeutics 42 (7): 793–801. https://doi. org/10.1111/apt.13344
Tenorio-Jiménez, C., M. J. Martínez-Ramírez, A. G., and C. Gómez-Llorente. 2020. "Effects of Probiotics on Metabolic Syndrome: A Systematic Review of Randomized Clinical Trials." Nutrients 12 (1): 124. https://doi.org/10.3390/ nu12010124
Wang, Y. H., N. Yao, K. K. Wei, L. Jiang, S. Hanif, Z. X. Wang, and C. X. Pei. 2016. "The Efficacy and Safety of Probiotics for Prevention of Chemoradiotherapy-Induced Diarrhea in People with Abdominal and Pelvic Cancer: A Systematic Review and Meta-Analysis." European Journal of Clinical Pharmacology 70 (11): 1246–1253. https://doi. org/10.1038/ejcn.2016.102
Wang, Z. B., S. S. Xin, L. N. Ding, W. Y. Ding, Y. L. Hou,
C. Q Liu, and X. D. Zhang. 2019. "The Potential Role of Probiotics in Controlling Overweight/Obesity and Associ- ated Metabolic Parameters in Adults: A Systematic Review and Meta-Analysis." Evidence-Based Complementary and Alternative Medicine 2019:3862971. https://doi. org/10.1155/2019/3862971
Zhang, C., J. Jiang, F. Tian, J. Zhao, H. Zhang, Q. Zhai, and W. Chen. 2020. "Meta-analysis of Randomized Controlled Trials of The Effects of Probiotics on Functional Constipa- tion in Adults." Clinical Nutrition 39 (10): 2960–69. https:// doi.org/10.1016/j.clnu.2020.01.005
Zhang, M. M., W. Qian, Y. Y. Qin, J. He, and Y. H. Zhou. 2015. "Probiotics in Helicobacter pylori Eradication Therapy: A Systematic Review and Meta-Analysis." World Journal of Gastroenterology 21 (14): 4345–57. https://doi. org/10.3748/wjg.v21.i14.4345
Zhang, Q., Y. Wu, and X. Fei. 2016. "Effect of Probiotics on Glucose Metabolism in Patients with Type 2 Diabetes Mel- litus: A Meta-Analysis of Randomized Controlled Trials." Medicina (Kaunas) 52 (1): 28–34. https://doi.org/10.1016/j. medici.2015.11.008
Zhang, Y., L. Li, C. Guo, D. Mu, B. Feng, X. Zuo, and Y. Li. 2016. "Effects of Probiotic Type, Dose and Treatment Duration on Irritable Bowel Syndrome Diagnosed by Rome III Criteria: A Meta-Analysis." BMC Gastroenterology 16 (1): 62. https://doi.org/10.1186/s12876-016-0470-z



