
Credit: Jim Newman, UF/IFAS
Resumen
Zika es un virus transmitido por mosquitos que se ha esparcido recientemente en regiones tropicales y ha causado epidemias, especialmente durante los últimos 8 o 9 años. En su ámbito nativo en África Occidental y Uganda, el virus se mantiene en los bosques, circulando entre mosquitos que viven en huecos de árboles y primates arbóreos; las infecciones de humanos se consideran incidentales y de poca importancia médica. Una cepa del virus que se implicó en brotes en Polinesia Francesa emergió en el Norte de Brasil en el 2015 y causó gran consternación debido a la alta incidencia de microcefalia en bebes nacidos de madres que fueron infectadas con el virus durante la gestación. Transmisión local, principalmente por el mosquito de la fiebre amarilla Aedes aegypti, ha sido documentada en la mayoría de los países tropicales de las Américas y en Los Estados Unidos Continentales. Los síntomas de la infección incluyen, salpullido, dolor de cabeza, fiebre, dolor muscular y en las coyunturas, conjuntivitis, y malestar general. Se recomienda obtener diagnosis definitiva por pruebas moleculares debido a que los síntomas se parecen a los de otras enfermedades virales. Ya que no existe vacuna contra el Zika, la mejor prevención es evitar las regiones donde el virus se transmite actualmente, y las picadas de mosquitos, especialmente por Aedes aegypti.
El virus Zika
La enfermedad Zika es causada por un virus de la familia Flaviviridae transmitido por artrópodos (arbovirus). Consiste de tres cepas (linajes), una de Asia y dos de África (Kuno et al. 1998, Faye et al. 2014). El virus Zika consiste de una molécula de ARN de cadena simple y sentido positivo de 10794 bases nucleotidas. Las especies de mosquitos Aedes se infectan con el virus al alimentarse de la sangre de un huésped vertebrado (simio o humano) y después de un periodo de incubación de varios días puede transmitir el virus al picar a otro vertebrado. El virus se aisló por primera vez en 1947 de un mono rhesus en el bosque Zika de Uganda. El ciclo selvático ocurre entre mosquitos Aedes que viven entre las copas de los árboles y monos (Hayes 2009), mientras que el ciclo urbano incluye mosquitos Aedes (el de la fiebre amarilla y el mosquito tigre Asiático) y humanos. El virus normalmente se transmite por picadas de mosquitos pero existen otros modos de transmisión. Madres infectadas con el virus Zika (ZIKV) puede pasar el virus al feto durante el embarazo (Besnard et al. 2014, Schuler-Faccini et al. 2016). El virus también puede ser transmitido por transfusiones de sangre y por contacto sexual (Foy et al. 2011, Musso et al. 2014). Se ha demostrado que el ZIKV está presente en la orina y la saliva, pero no se sabe si puede ser transmitido a través de estos fluidos.
El ZIKV tradicionalmente circulaba solo en ciclos Africanos y en partes del sureste asiático, y antes del 2007 solo se conocían 14 casos humanos (Duffy et al. 2009, Hayes et al., 2009). El virus ha manifestado una expansión geográfica durante la última década, durante la cual se ha expandido a islas del Pacífico (desde el 2007) y a las Américas (desde el 2015; ECDC 2015), donde ha causado epidemias de la enfermedad Zika. Un extenso brote de Zika causado por la cepa Asiática tuvo lugar en Polinesia Francesa en 2013-2014 (Lanciotti et al. 2007, Musso 2015) y luego se extendió a otras islas del Pacífico (Musso et al. 2015). Luego, ZIKV se extendió a Brasil, quizás debido a viajes internacionales asociados con competencia olímpicas en Brasil (Zanluca et al. 2015). Los brotes en las Américas también son atribuidos a la cepa Asiática de ZIKV.
Los mosquitos vectores del virus Zika
El ciclo Africano entre primates arbóreos y mosquitos es mantenido principalmente por los mosquitos Aedes africanus en Uganda (Haddow et al. 1964), y Aedes furcifer, Aedes luteocephalus, y Aedes africanus en Senegal (Diallo et al. 2014). Aedes furcifer machos infectados con ZIKV y atrapados en el bosque son evidencia de que el virus puede ser transmitido de una hembra mosquito infectada a su cría a través de los huevos. (Diallo et al. 2014).
Pruebas serológicas demuestran que infecciones humanas con ZIKV puede ser comunes, por ejemplo, 40% de una población urbana examinada en Nigeria poseía los anticuerpos contra el virus (Fagbami 1979). Durante infecciones en habitas domésticos colaterales al ciclo selvático, se han encontrado otras especies de Aedes infectadas con ZIKV, por ejemplo, Aedes metallicus y Aedes vittatus en Senegal (Diallo et al. 2014). No está claro el significado epidemiológico de aislamientos de ZIKV de mosquitos de otros géneros, especialmente especies de los géneros Mansonia, Culex, y Anopheles.
En el ámbito invasivo del virus fuera de África, incluyendo las Américas, el vector más probable es Aedes aegypti (Figura 1), en el cual se encontró la infección por primera vez en su hábitat natural en Malasia (Marchette et al. 1969). La predilección de Aedes aegypti por sangre humana en ciudades en los trópicos supera su relativa ineficiencia para desarrollar al virus (Diagne et al. 2015). Aedes albopictus (Figura 1), un mosquito que expandido su ámbito mundialmente, ha sido implicado como un vector de ZIKV en Gabón (Grad et al. 2014). Esto adquiere mayor importancia según el mosquito y el virus expanden sus distribuciones por todo el mundo lo cual causa cohabitación del virus con poblaciones del mosquito que se alimentan en humanos. En Micronesia, el mosquito Aedes hensilli fue el más probable vector de la epidemia de 2007 en las Islas Yap.
No sabemos aún cuales mosquitos nativos de las Américas podrán ser vectores del Zika (ambos Aedes aegypti y Aedes albopictus son invasores de África y Asia, respectivamente). Se justifica la preocupación de que ZIKV se vuelva endémico en boques tropicales del Nuevo Mundo en ciclos de transmisión entre mosquitos arbóreos que viven en los huecos de árboles, tales como especies de Haemagogus y Sabethes, y primates neo-tropicales no humanos, así como ocurrió siglos antes en Suramérica y Centroamérica con el virus de la fiebre amarilla después de su introducción y difusión de África (Barret y Higgs 2007). Aún no se puede confirmar la importancia relativa de diferentes especies de vectores en la actual epidemia en las Américas, pero hay gran probabilidad de que Aedes aegypti y Aedes albopictus sean las especies más importantes. Si es así, esto debe aumentar la preocupación con Zika en sitios donde estas especies ocurren.
La enfermedad con el virus Zika
Sintomas: Los síntomas incluyen fiebre con inicio súbito, salpullido, dolor de cabeza, dolor muscular y en las coyunturas, conjuntivitis, y malestar general. Hasta hace poco, la enfermedad se caracterizó como clínicamente leve. Los síntomas primarios duran de varios días a una semana, gran proporción de las infecciones (80%) son asintomáticas (CDC 2016), y raramente hay necesidad de hospitalización. Sin embargo, durante el brote de Zika del 2013 en Polinesia Francesa se implicó el ZIKV en trastornos neurológicos asociados con el síndrome Guillain-Barré, y la epidemia actual de Zika en Brasil implica al ZIKV con un aumento significativo en el número de bebes nacidos con microcefalia (ECDC 2015, PAHO/WHO 2015, 2016).
Diagnosis: Infecciones con Zika so difíciles de diagnosticar ya que los síntomas son parecidos a los de otras enfermedades causadas por arbovirus y muy pocos laboratorios hacen las pruebas moleculares necesarias. Fuera de áreas donde hay transmisión actual, diagnosis preliminar incluye determinación del historial de viajes del paciente. Pruebas de laboratorio incluyen la detección del ácido nucleico del virus en suero (usando reacción en cadena de polimerasa con transcriptasa inversa) durante el comienzo de los síntomas. Después de la primera semana con síntomas, anticuerpos IgM (detectados vía ELISA) y pruebas de neutralización por reducción en placas (pruebas que miden el título de anticuerpos neutralizantes contra un virus) se pueden utilizar para verificar contacto con el virus (Duffy et al. 2009, CDC 2016). El virus Zika se puede detectar en el cuerpo humano desde el día en que aparecen los síntomas, y el ARN del virus se puede detectar hasta 11 días después del inicio de los síntomas (Lanciotti et al. 2008).
Tratamiento: No existen vacunas ni medicinas específicas para el tratamiento de infección con ZIKV. Solo se recomienda tratamiento de apoyo (descanso, líquidos, y medicinas como el acetaminofén para el dolor y la fiebre). Los enfermos no deben tomar aspirina ni otros productos antiinflamatorios no esteroideos antes de eliminar la posibilidad de tener dengue, ya que estos productos pueden agravar la pérdida de sangre asociada con algunas formas de dengue (CDC 2016).
Zika y microcefalia: Puede existir una relación entre la presencia del virus Zika y la microcefalia congénita en bebes recién nacidos. Microcefalia es un infrecuente trastorno neurológico que causa que la cabeza del recién nacido sea más pequeña que lo usual, debido al desarrollo anormal del cerebro en el útero. En octubre del 2015, el Ministerio de Salud de Brasil reportó un aumento en el número de bebes nacidos con microcefalia que coincidía con el brote de Zika en mayo (ECDC 2015, PAHO/WHO 2015, 2016). Evidencia de ZIKV se descubrió en el líquido amniótico de dos mujeres embarazadas cuyos fetos fueron diagnosticados en utero con microcefalia; el virus luego fue reconocido en el cerebro de los recién nacidos y en las placentas (PAHO/WHO 2015). Sin embargo, hasta ahora no se ha establecido un vínculo definitivo entre la microcefalia y la infección con ZIKV (Fauci y Morens 2016). Durante el brote actual (2015-2016) de Zika, varias agencias relacionadas con la salud pública, incluyendo Los Centros para el Control y Prevención de Enfermedades de E.U. (CDC) aconsejaron que mujeres embarazadas no viajen a sitio donde hay transmisión activa del virus.
Zika y el síndrome Guillain-Barré: El síndrome Guillain-Barré (SGB) ocurre cuando el sistema autoinmune de una persona ataca las células del sistema nervioso lo cual causa debilidad muscular y algunas veces parálisis. En Los Estados Unidos normalmente ocurren de 3,000 a 6,000 casos de SGB anualmente.
Las causas de SGB no son bien conocidas, pero muchos casos de la enfermedad ocurren poco después de una infección con virus o bacteria. SGB se ha relacionado con infecciones por un gran número de patógenos, incluyendo virus acarreados por mosquitos como los del dengue y chikungunya (Lebrun et al. 2009, Oehler et al. 2015). En Polinesia, SGB está relacionado con infecciones previas con ZIKV y la incidencia de SGB aumentó durante la epidemia de Zika (Oehler et al. 2014); muchos de los pacientes con SGB también tuvieron síntomas consistentes con infección con Zika (PAHO 2016). Casos recientes de SGB en Brasil surgieron luego de infección con ZIKV, y El Salvador ha declarado un aumento inusual en SGB desde diciembre 2015 (PAHO 2015). Las causas fundamentales de SGB y su específica conexión con Zika o con otras infecciones causadas por arbovirus son por ahora desconocidas.
Historia del virus Zika
El virus debe su nombre al Bosque Zika, donde fue descubierto por primera vez por científicos del Instituto de Investigación sobre La Fiebre Amarilla, en Entebbe, Uganda. Muestras iniciales se obtuvieron no solo del mono enjaulado en el bosque, sino también de mosquitos Aedes africanus, capturados por cebos humanos (Dick et al. 1952). Las muestras del virus, y la ausencia de evidencia del virus en mamíferos capturados en el bosque llevaron a la hipótesis de que, similarmente al ciclo selvático del virus de la fiebre amarilla, Zika se mantenía naturalmente entre primates arbóreos y especies de mosquitos tropicales que normalmente se alimentaban con sangre en las copas de los árboles (Haddow et al. 1964). Los escasos reportes de casos humanos se consideraron callejones sin salida que no contribuían al ciclo natural de Zika (Simpson 1964).
Más tarde, ZIKV se identificó en varios países del centro y oeste de África, donde también se creía que persistía en ciclos selváticos entre mosquitos y huéspedes simios. Análisis moleculares de los linajes del virus sugieren dos diferentes introducciones de Uganda a África Occidental, la primara comenzando cerca del 1935 y la segunda cerca del 1940 (Faye et al. 2014; Figura 2).
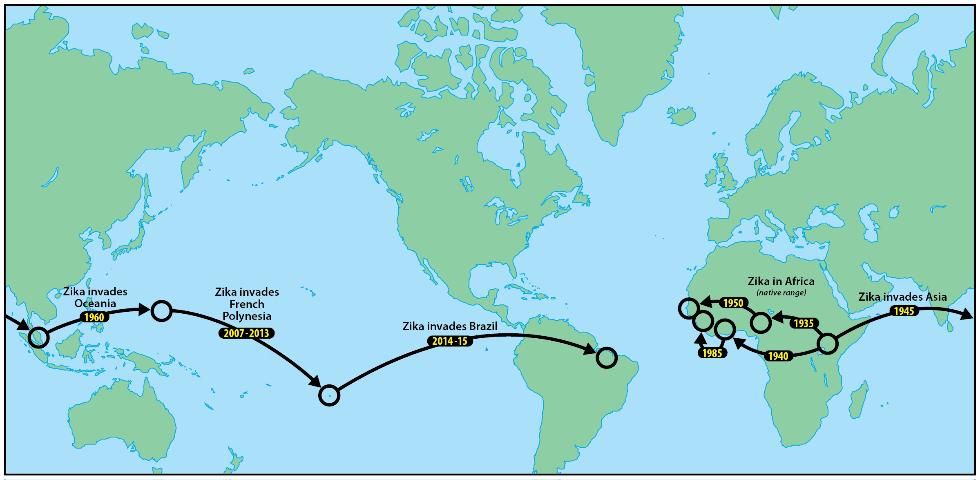
Credit: J. Newman, UF/IFAS/FMEL
El surgimiento de Zika fuera de África coincidió con un cambio aparente en el ciclo principal de transmisión de uno selvático entre monos y mosquitos donde el hombre jugaba un rol incidental, a uno donde el hombre era el huésped principal y el virus era propagado principalmente por mosquitos domésticos o peri-domésticos, por ejemplo, las especies invasivas Aedes aegypti y Aedes albopictus.
En el 2013, un gran brote de Zika en Polinesia Francesas, también debido a linaje Asiático, ocurrió después de la epidemia en las Islas Yap (Cao-Lormeau et al. 2014). Se sospecha que la epidemia que comenzó en el norte de Brasil en el 2015 (Campos et al. 2015) fue iniciada por la introducción de ZIKV por un viajero de Polinesia (Musso 2015). Actualmente hay transmisión activa de ZIKV en más de 20 países tropicales en las Américas, además de Estados Unidos Continentales, Puerto Rico y las Islas Vírgenes de E.U. (CDC 2016).
Zika en Florida
Al momento de esta publicación, se ha reportado transmisión local de ZIKV en Los Estados Unidos en Texas (por contacto sexual), Puerto Rico, Islas Vírgenes, y Samoa Americana. En Florida han ocurrido múltiples casos importados de Zika asociados con viajes a Colombia, El Salvador, Haití, y Venezuela. Para el 5 de febrero del 2016 se reportaron cuatro casos en el condado Miami-Dade, dos en Hillsborough, dos en Lee, y uno de Santa Rosa (FDOH 2016). Por ahora no existe evidencia de transmisión local propagada por mosquitos de Florida.
La expansión geográfica de Zika, especialmente en las Américas constituye un riesgo para Florida debido a: 1) un aumento en los casos importados por viajeros a Florida, un estado con mucho turismo; 2) una alta población susceptible al virus, especialmente en áreas urbanas; 3) condiciones ambientales conductivas al desarrollo de mosquitos y a la replicación del virus, especialmente durante la temporada lluviosa; 4) abundancia de los vectores Aedes aegypti y Aedes albopictus en estrecha asociación con humanos en gran parte del Estado. Entre los años 2007-2014 hubo solo 14 casos de Zika importados a Florida. La expansión del virus a las Américas ha resultado en un aumento en los casos importados al país. El importe de casos aumenta el riesgo de que se establezca transmisión local debido a que el virus circula en la sangre por varios días durante cual periodo el viajero enfermo puede transmitir el virus a mosquitos locales, que a su vez, pueden transmitirlo a otras personas.
Prevención contra infección con el virus Zika
No hay vacunas que protejan contra el virus Zika así que protegerse contra las picadas de mosquitos es el mejor método de prevención. Dado a la evidencia de que ZIKV puede ser transmitido por contacto sexual se recomienda que parejas tomen precauciones adecuadas (ver https://www.cdc.gov/media/releases/2016/s0205-zika-interim-guidelines.html). Se está trabajando en desarrollar vacunas contra el ZIKV, pero estas no estarán disponible por varios años. La protección contra picadas de mosquito supone protección personal y reducción de las poblaciones de mosquitos.
La protección personal se logra usando repelentes adecuados y ropa protectora, y evitando los sitios donde los mosquitos son abundantes. Los Centros para el Control y Prevención de Enfermedades facilitan una lista de repelentes que contienen ingredientes registrados con la Agencia para Protección del Ambiente ("Environmental Protection Agency", EPA) así como DEET, picaridin, y aceite de eucalipto que proveen protección duradera (https://www.cdc.gov/westnile/esp/prevencion/index_en_espanol.html).
Fuera de África, las especies de mosquito que propagan el ZIKV prosperan en áreas urbanas y sub-urbanas. Las larvas se desarrollan en aguas que se acumulan en recipientes naturales y artificiales tales como huecos en árboles, baños de aves, jarrones, macetas, cubos, llantas desechadas, latas vacías, y muchos otros recipientes desechados y olvidados (Rey y Connelly 2013). Descartando o vaciando estos recipientes regularmente es buena manera de reducir las poblaciones de mosquitos que transmiten Zika (Connelly et al. 2014; https://edis.ifas.ufl.edu/publication/in1045). Recipientes permanentes tales como los huecos de árbol o barriles para coleccionar agua de lluvia se deben llenar con arena o cemento (huecos), o tapar con tela metálica (barriles).
En Estados Unidos, es mandatorio reportar a autoridades de salud pública (del estado o al CDC) si se sospecha que un paciente padece de infección con ZIKV. Esta información generalmente se distribuye a las autoridades indicadas, incluyendo a las agencias para el control de mosquitos. Agencias para el control de mosquitos pueden tomar medidas para reprimir poblaciones locales de mosquitos en sitios donde se sospecha que existe transmisión local de Zika. En Florida, estas agencias también pueden suministrar información adicional sobre los mosquitos que transmiten ZIKV para ayudar en la determinación de riesgos locales. El Laboratorio de Entomología Médica de Florida ("Florida Medical Entomology Laboratory") un centro de investigación y educación de la Universidad de Florida que se especializa en investigación sobre patógenos transmitidos por mosquitos provee una lista de los 61 programas de control de mosquitos en el Estado (https://fmel.ifas.ufl.edu/florida-mosquito-control/florida-mosquito-control-table-by-county/).
Referencias
Ahmed, A. 2016. "One country's advice on Zika virus: don't have babies." New York Times 25 January 2016.
Barrett, A. D. H., and S. Higgs. 2007. "Yellow fever: a disease that has yet to be conquered." Annual Review of Entomology 52: 209–229.
Besnard, M., S. Lastère, A. Teissier, V. M. Cao-Lormeau, and D. Musso. 2014. "Evidence of perinatal transmission of Zika virus, French Polynesia, December 2013 and February 2014." Euro. Surveill. 19(13): ppii: 20751.
Campos, G. S., A. C. Bandeira, and S. I. Sardi. 2015. "Zika virus outbreak, Bahia, Brazil." Emerging Infectious Diseases 21: 1885–1886.
Cao-Lormeau, V-M., C. Roche, A. Tessier, E. Robin, A-L. Berry, H-P. Mallett, A. A. Sall, and D. Musso. 2014. "Zika virus, French Polynesia, South Pacific, 2013." Emerging Infectious Diseases 20: 1085–1086.
Carod-Artal, F., O. Wichmann, J. Farrar, and G. Joaquim. 2013. "Neurological complications of dengue virus infection." Lancet Neurol. 12: 906–16
Centers for Disease Control and Prevention (CDC). 2016. Zika Virus. National Center for Emerging and Zoonotic Infectious Diseases (NCEZID). https://www.cdc.gov/zika/ (accessed 14 April 2022)
Connelly, C. R., E. Bolles, D. Culbert, J. DeValerio, M. Donahoe, K. Gabel, R. Jordi, J. McLaughlin, A. S. Neal, S. Scalera, E. Toro, and J. Walter. 2014. Integrated Pest Management for Mosquito Reduction around Homes and Neighborhoods. https://edis.ifas.ufl.edu/publication/in1045 (accessed 14 April 2022)
Diagne, C. T., D. Diallo, O. Faye, Y. Ba, O. Faye, A. Gaye, I. Dia, O. Faye, S. C. Weaver, A. A. Sall, and M. Diallo. 2015. "Potential of selected Senegalese Aedes spp. mosquitoes (Diptera: Culicidae) to transmit Zika virus." BMC Infectious Diseases 15: 492.
Diallo, D., A. A. Sall, C. T. Diagne, O. Faye, O. Faye, Y. Ba, K. A. Hanley, M. Buenemann, S. C. Weaver, and M. Diallo. 2014. "Zika virus emergence in mosquitoes in southeastern Senegal." PLoS One 9(10): e109442.
Dick, G. W. A., S. F. Kitchen, and A. J. Haddow. 1952. "Zika virus." Transactions of the Royal Society of Tropical Medicine and Hygiene. 46: 509–534.
Duffy, M. R., T-H. Chen, W. T. Hancock, A. M. Poers, J. L. Kool, R. S. Lanciotti, M. Pretrick, M. Marfel, S. Holzbauer, C. Dubiay, L. Guillaumot, A. Griggs, M. Bel, A. J. Lambert, J. Laven, O. Kosoy, A. Panella, B. J. Biggerstaff, M. Fischer, and E. B. Hayes. 2009. "Zika virus outbreak on Yap Island, Federated States of Micronesia." New England Journal of Medicine 360: 2536–43.
[ECDC] European Centre for Disease Prevention and Control. 2015. Rapid risk assessment: Zika virus epidemic in the Americas: potential association with microcephaly and Guillain-Barré syndrome. 10 December 2015. Stockholm: ECDC, 2015.
Fagbami, A. H. 1979. "Zika virus infections in Nigeria: virological and seroepidemiological investigations in Oyo State." The Journal of Hygiene 83:213–219.
Fauci, A. S., and D. M. Morens. 2016. "Zika Virus in the Americas — Yet Another Arbovirus Threat." The New England Journal of Medicine. DOI: 10.1056/NEJMp1600297
Faye, O., C. C. M. Freire, A. Lamarino, O. Faye, J. V. C. de Oliveira, M. Diallo, P. M. A. Zanotto, and A. A. Sall. 2014. "Molecular evolution of Zika virus during its emergence in the 20th century." PLoS Neglected Tropical Disease 8(1): e2636.
Florida Department of Health. 2016. https://www.floridahealth.gov/diseases-and-conditions/mosquito-borne-diseases/_documents/week4arbovirusreport-1-30-16.pdf (site visited April 14, 2022).
Foy, B. D., K. C. Kobylinski, J. L. Chilson Foy, B. J. Blitvich, A. Travassos da Rosa, et al. 2011. "Probable non-vector-borne transmission of Zika virus, Colorado, USA." Emerg. Infect. Dis. 17(5):880–882.
Grard, G., M. Caron, I. M. Mombo, D. Nkoghe, S. M. Ondo, D. Jiolee, D. Fontenille, C. Paupy, and E. M. Leroy. 2014. "Zika virus in Gabon (Central Africa)-2007: a new threat from Aedes albopictus?" PLoS Neglected Tropical Diseases 8(2): e2681.
Haddow, A. J., M. C. Williams, J. P. Woodall, D. I. H. Simpson, and L. K. H. Goma. 1964. "Twelve isolates of Zika virus from Aedes (Stegomyia) africanus (Theobald) taken in and above a Uganda forest." Bulletin of the World Health Organization. 31: 57–69.
Hayes, E. B.. 2009. "Zika virus outside Africa." Emerging Infectious Diseases 15: 1347–1350.
Kuno, G., G. J. Chang, K. R. Tsuchiya, N. Karabatsos, and C. B. Cropp. 1998. "Phylogeny of the genus Flavivirus." J. Virol. 72(1):73–83.
Lanciotti, R. S., O. L. Kosoy, J. J. Laven, J. O. Velez, A. J. Lambert, A. J. Johnson, S. M. Stanfield, and M. R. Duffy. 2008. "Genetic and serologic properties of Zika virus associated with an epidemic, Yap State, Micronesia, 2007." Emerg. Infect. Dis. 14(8):1232–1239.
Lebrun, G., K. Chadda, A. Reboux, O. Martinet, and B. Gaüzère. 2009. "Guillain-Barré syndrome after Chikungunya infection." EID 15: 495–496.
Marchette, N. J., R. Garcia, and A. Rudnick. 1969. "Isolation of Zika virus from Aedes aegypti mosquitoes in Malaysia." American Journal of Tropical Medicine and Hygiene 18: 411–415.
Mayo Clinic. 2016. Disease and Conditions: Microcephaly. https://www.mayoclinic.org/diseases-conditions/microcephaly/symptoms-causes/syc-20375051
Musso, D. 2015. "Zika virus transmission from French Polynesia to Brazil." Emerging Infectious Diseases 21: 1887.
Musso, D., V. M. Cao-Lormeau, and D. Gubler. 2015. "Zika virus: following the path of dengue and chikungunya?" Lancet 386(9990):243–44.
Musso, D., T. Nham, E. Robin, C. Roche, D. Bierlaire, K. Zisou, A. Shan Yan, V. M. Cao-Lormeau, and J. Broult. 2014. "Potential for Zika virus transmission through blood transmission demonstrated during an outbreak in French Polynesia, November 2013 to February 2014." Euro Surveill. 19(14): ppii: 20761.
National Institutes of Health. NIH GBS fact sheet. https://www.ninds.nih.gov/health-information/disorders/guillain-barre-syndrome (accessed 1 January 2023)
Oehler, E., L. Watrin, P. Larre, I. Leparc-Goffart, S. Lastère, F. Valour, L. Baudouin, H. P. Mallet, D. Musso, and F. Ghawche. 2014. "Zika virus infection complicated by Guillain-Barré syndrome – case report, French Polynesia, December 2013." Euro Surveill. 19(9):pii=20720. Article DOI: https://doi.org/10.2807/1560-7917.ES2014.19.9.20720
Oehler, E., E. Fournier, I. Leparc-Goffart, P. Larre, S. Cubizolle, C. Sookhareea, S. Lastère, and F. Ghawche. 2015. "Increase in cases of Guillain-Barré syndrome during a Chikungunya outbreak, French Polynesia, 2014 to 2015." Euro Surveill. 20(48):pii=30079. DOI: https://doi.org/10.2807/1560-7917.ES.2015.20.48.30079 (accessed 5 February 2016)
Pan American Health Organization, World Health Organization. Regional Office for the Americas. 2015. Epidemiological Alert: Increase of microcephaly in the northeast of Brazil. https://iris.paho.org/handle/10665.2/50666
PAHO/WHO. 2016. Epidemiological update: neurological syndrome, congenital anomalies and Zika virus infection. https://iris.paho.org/handle/10665.2/50659.
Rey, J. R., and C. R. Connelly. 2013. Florida Container Mosquitoes. https://edis.ifas.ufl.edu/in851 (accessed 5 February 2016)
Schuler-Faccini, L., E. M. Ribeiro, I. M. L. Feitosa, D. D. G. Horovitz, D. P. Cavalcanti, et al. 2016. "Possible association between Zika virus infection and microcephaly – Brazil, 2015." MMWR Morb. Mortal. Wkly. Rep. 65(3):59–62.
Simpson, D. I. H. 1964. "Zika virus infection in man." Tropical Medicine and Hygiene 58: 335–338.
Zanluca, C., V. C. A. de Melo, A. L. P. Mosimann, G. I. V. dos Santos, C. N. D. dos Santos, and K. Luz. 2015. "First report of autochthonous transmission of Zika virus in Brazil." Mem Inst Oswaldo Cruz. 110(4):569–572.