La colección Featured Creatures proporciona perfiles detallados de insectos, nematodos, arácnidos y otros organismos relevantes para Florida. Estos perfiles están destinados al uso del público académico así como el de cualquier persona con algún conocimiento de biología.
Introducción
El taladrador de las meliáceas, Hypsipyla grandella (Zeller), taladra los brotes de árboles en la familia de las meliáceas (Meliaceae), especialmente las caobas (Swietenia spp.) y los cedros (Cedrela spp.). Desde el punto de vista de la economía, es una plaga importante, y ha sido el objetivo de investigaciones en muchos países tropicales. Es la única especie de Hypsipyla en Florida, donde es una plaga de la caoba antillana (Swietenia mahagoni Jacquin), un árbol nativo que se planta frecuentemente como árbol de sombra.

Crédito: Doug Caldwell, UF/IFAS
El Hypsipyla robusta (Moore) y las especies cercanas en Madagascar y África juegan un papel similar al del taladrador de brotes de árboles meliáceos en regiones tropicales del hemisferio oriental. Actualmente, se entiende que Hypsipyla robusta es un complejo de especies y su taxonomía está siendo resuelta (Marianne Horak, comunicación personal). Para referirse al Hypsipyla robusta y tal vez a otras especies de este complejo se recurre a varios nombres vernáculos en inglés, los cuales pueden traducirse al español como taladrador de toona, polilla del brote del cedro, gusano del brote del cedro y en algunos países como el taladrador de caoba. En este artículo, el nombre taladrador de las meliáceas se refiere a la especie de las Américas, H. grandella. Se han descrito nueve especies adicionales de Hypsipyla. Todas son tropicales (tres en las Américas y seis en el hemisferio oriental). La distribución de cada una de esas es limitada, no son plagas económicas importantes y se conoce poco respecto a su biología (Horak 2001). Las revisiones recientes de taladradores Hypsipyla incluyen las de Newton et al. (1993) y Griffiths (2001). Los libros sobre las caobas con discusiones sobre los insectos asociados incluyen Lamb (1966) y Mayhew and Newton (1998) y treinta y seis trabajos fueron publicados en 'Proceedings of a Workshop on Hypsipyla shoot borers' (Floyd and Hauxwell 2001).
Distribución
La distribución del taladrador de las meliáceas probablemente coincide con la de sus plantas hospederas principales (esto es, las caobas y los cedros) i.e., el sur de la Florida, la mayoría de las islas de las Indias Occidentales, México desde Sinaloa hasta el sur, Centroamérica y América del Sur con la excepción de Chile (Griffiths 2001) (vea la sección de este texto: Plantas hospederas).
Descripción
Según Ramirez Sanchez (1964), Becker (1976), Solomon (1995):
Adulto
Los adultos de H. grandella son de color marrón a marrón-grisáceo. La envergadura de las alas anteriores es cerca de 23 a 45 mm. Estas son marrón-grisáceas sombreadas de color ladrillo en la parte posterior. El área media hacia afuera de las alas anteriores está espolvoreada con escamas y puntos negros hacia las puntas de las alas. Las venas de las alas están recubiertas con escamas negras. Las alas traseras son de blancas a translúcidas con márgenes oscuros. La cabeza, cuerpo y patas son de un color castaño-grisáceo.

Crédito: L. J. Buss, UF/IFAS
Huevo
Los huevos del taladrador de las meliáceas son ovalados, aplanados y miden aproximadamente 0,9 mm de largo por 0,5 mm de ancho. El color de los huevos cambia de blanco a rojizo dentro de las 24 horas posteriores a la oviposición.
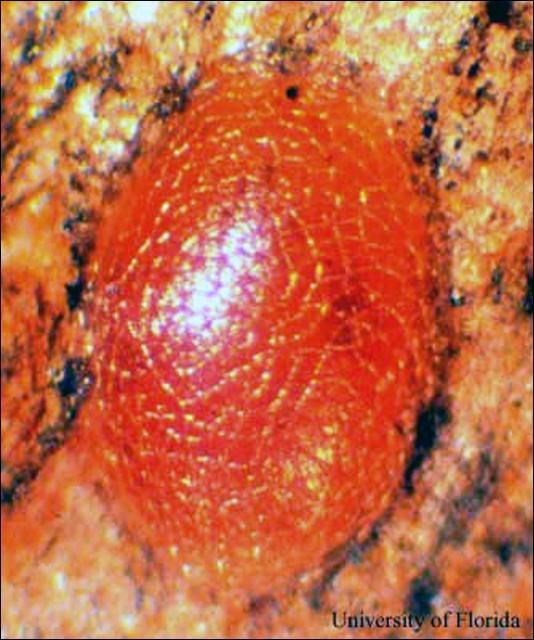
Crédito: J. V. DeFilippis, UF/IFAS
Larva
El cuerpo de la larva de los instares jóvenes es de un color café pálido a blanco, que se vuelve azul en los instares más avanzados. La cápsula de la cabeza es marrón. Las larvas maduras son de aproximadamente 25 mm de largo.

Crédito: F. W. Howard, UF/IFAS
Pupa
La pupa de H. grandella es de color marrón-negro y está envuelta en un capullo de seda.
Biología
Las polillas adultas son nocturnas y viven de siete a ocho días (Holsten 1976). Estas depositan los huevos durante las horas tempranas de la mañana sobre brotes nuevos, cicatrices de las hojas caídas, hojuelas (especialmente al lado de una vena en la superficie superior) y frutas. Los huevos generalmente se ponen uno por uno, pero a veces están agregados en un grupo de tres o cuatro huevos metidos en las axilas de hojas. Una hembra puede poner cerca de 300 huevos, pero típicamente pone no más que unos pocos huevos por cada árbol (Solomon 1995).
En estudios del tiempo de desarrollo del taladrador de las meliáceas alimentándose sobre las hojas frescas de cedro a temperaturas constantes, se encontró que la duración del estado larval variaba entre 30 (30°C) y 104 días (15°C) (Taveras et al. 2004). En el campo, la duración total del desarrollo de la larva, prepupa y pupa se completa de uno a dos meses, dependiendo de las condiciones ambientales, y puede extenderse si el insecto pasa por diapausa. Las larvas recientemente emergidas muchas veces empiezan a alimentarse de la superficie de la hoja o del brote, después taladran los brotes o las cápsulas de las semillas. Las larvas que taladran los brotes producen un túnel de varios centímetros de largo. El tallo hueco se seca y se dobla, y las hojas de este se mueren. Una masa de excremento de color marrón-rojizo entrelazado con hilos de seda del insecto sale de la apertura de entrada. Se puede determinar por la apariencia del excremento expelido si una larva está taladrando activamente un brote, pues este es compacto y relativamente pálido en color, y se vuelve más oscuro y desintegrado después de que la larva ya no está alimentándose (por ejemplo, en el estado de pupa) (Howard 1991). Al partir una ramita o brote infestado, se puede observar la larva o pupa, si alguna de estas está adentro.

Crédito: F. W. Howard, UF/IFAS

Crédito: Jim DeFilippis, UF/IFAS
Los taladradores de las caobas atacan brotes nuevos, raramente atacan los brotes maduros. En el sur de Florida, donde el brote de la caoba antillana se lleva a cabo durante abril-junio (Howard 1991), los taladradores de caobas atacan los brotes desde principios de primavera hasta mitad del verano, con picos poblacionales en mayo. En los trópicos, el taladrador de las meliáceas está activo todo el año y la actividad se concentra en la temporada de lluvias, la cual es el período de crecimiento de brotes de las caobas. Se han observado picos poblacionales en la primavera, i.e., en el principio de la temporada de lluvias (Roovers 1971; Bauer 1987).

Crédito: F. W. Howard, UF/IFAS
El taladrador de las meliáceas también ataca las cápsulas de las semillas de las caobas, los cedros, y otros árboles meliáceos. Según observaciones sobre el ataque de este insecto a caobas antillanas en el sur de la Florida, raramente perforan las válvulas duras de las cápsulas de las semillas, sino que penetran a ellas cuando la cápsula abre. En este sitio consumen las 50–80 semillas, luego penetran el corazón de la cápsula donde a veces pasan el estado de la pupa. En la Florida, el ataque del taladrador de las meliáceas a cápsulas de semilla de la caoba antillana esta básicamente limitado al período durante la dehiscencia de la cápsula, eso es, en la primavera, antes y simultaneámente con la producción de nuevos brotes (Howard and Gilblin-Davis 1997). El estadio de la pupa toma lugar dentro del brote hueco o sea en la cápsula de semillas, u ocasionalmente en la capa de hojas muertas o en el suelo debajo los árboles hospederos. El estadio de la pupa dura 8–10 días (Ramírez Sánchez 1964).
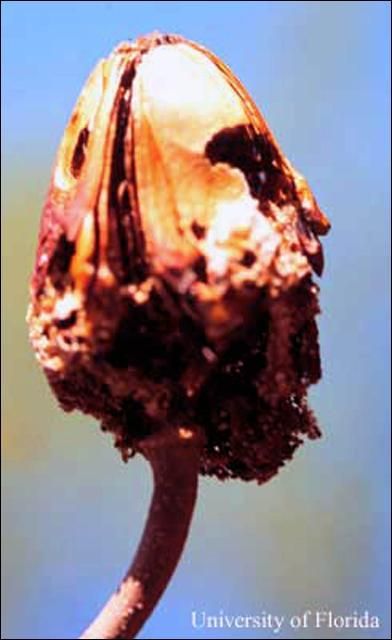
Crédito: F. W. Howard, UF/IFAS

Crédito: F. W. Howard, UF/IFAS
Plantas hospederas
Especies de varios géneros en la familia botánica Meliaceae sirven como plantas hospederas del taladrador de las meliáceas, incluyendo Carapa, Cedrela, Guarea, Khaya, Swietenia, y Trichilia (Entwistle 1967; Becker 1976). La mayoría de las especies son nativas de los trópicos de las Américas, pero especies exóticas a estas regiones como la Khaya spp. pueden ser atacadas cuando se plantan en la América Tropical.
Entre las especies nativas, la Cedrela odorata L. tiene la distribución más amplia, en las áreas continentales de las Américas desde el norte de México hasta la Argentina, y en la mayoría de las islas de las Indias Occidentales (Cintron 1990). El rango de esta especie más o menos coincide con la del taladrador de las meliáceas, con la excepción de que el C. odorata no es nativo de la Florida. Hay por lo menos 11 especies de Cedrela (Pennington 1981), y se sabe que el taladrador de las meliáceas ataca por lo menos a algunas de ellas además de atacar al C. odorata (Becker 1976). Los cedros son árboles de crecimiento rápido y son grandes en la madurez. Su madera se utiliza localmente de diferentes maneras a lo largo de las zonas tropicales americanas, y se plantan como árboles de sombra en áreas urbanas de esta región, pero están presentes solamente como especímenes de árboles ocasionales en la Florida.

Crédito: F. W. Howard, UF/IFAS
El nombre vernáculo del taladrador de las meliáceas de la caoba refleja la importancia comercial de unas de sus plantas hospederas, eso es, las caobas. Las caobas verdaderas (Swietenia spp.) son nativas de las zonas tropicales americanas y de algunas áreas fuera de las zonas tropicales con un clima tropical, tales como las Bahamas y la Florida meridional. El género incluye las tres especies siguientes (Record and Hess 1943; Lamb 1966; Pennington 1981):
La caoba de las Indias Occidentales (S. mahagoni [Jacquin]), que es nativa a la Florida meridional, las Bahamas, y las Antillas Mayores excepto Puerto Rico. Éste es uno de los árboles más populares para uso ornamental o para sombra en áreas urbanas de la Florida meridional, y es un componente de bosques naturales de áreas tales como los Everglades y Los Cayos de la Florida. Es el único árbol meliáceo grande que es común en la Florida.

Crédito: F. W. Howard, UF/IFAS

Crédito: F. W. Howard, UF/IFAS

Crédito: F. W. Howard, UF/IFAS
La caoba hondureña (S. macrophylla King), que es nativa del continente, de la América Tropical, y se da en regiones húmedas tropicales desde alrededor de una latitud de 22° N en el lado atlántico de México a lo largo de Centroamérica y de Sudamérica hasta alrededor de la latitud 22° S en Bolivia. Es actualmente la fuente principal de la madera de caoba, pero en la Florida se encuentra solamente como un espécimen ocasional..

Crédito: F. W. Howard, UF/IFAS
La caoba del Pacífico (S. humilis Zuccarini) que se distribuye en una franja a lo largo de las áreas costeras del Pacífico desde México hasta Costa Rica. En la Florida es un espécimen de árbol que rara vez se ve.
Las caobas son quizás los árboles maderables tropicales más importantes del mundo. La madera se usa principalmente para muebles. Durante la época de la Colonia en el Caribe, la caoba antillana fue explotada extensivamente, y después la caoba hondureña, la cual se distribuye más ampliamente en el continente americano, se convirtió en la fuente principal de la madera de caoba.
Ciertas especies de árboles meliáceos que son nativas a las zonas tropicales del hemisferio oriental son atacadas por el taladrador de las meliáceas (H. grandella) cuando dichas plantas se siembran como exóticas en las Américas; en sus regiones nativas son generalmente plantas hospederas de la contraparte de este insecto en el Hemisferio Oriental, eso es, H. robusta. Un ejemplo es la caoba de Nyasalandia, o caoba africana (Khayanyasica Baker ex f de Stapf.) (Entwistle 196; Becker 1976).
No obstante, el cedro-rojo (Toona ciliata [ Roemer ] var. australis), y la caoba africana (Khaya ivorensis A. Chevallier), ambos árboles meliáceos maderables importantes de las zonas tropicales del hemisferio oriental que son atacadas fuertemente por el H. robusta al crecer allí, no fueron atacadas por H. grandella cuando se desarrollaron en Costa Rica (Grijpma 1970).
Daños económicos
Los árboles de caoba son susceptibles al ataque cuando alcanzan una altura de 0,5 m (Griffiths 2001), aunque en la Florida raramente son atacados cuando tienen menos de 1 m de alto (Howard, inéditos). El daño más severo del insecto a los árboles ocurre cuando una larva taladra en el brote terminal y lo mata. Un ramo lateral crece hacia arriba para substituir al brote terminal perdido, dando por resultado un tallo principal torcido. También el daño al terminal rompe la dominación apical, dando por resultado una ramificación lateral excesiva (Howard and Meerow 1993). Los árboles pequeños cuyos brotes terminales son atacados repetidamente en años sucesivos se deforman de manera extrema.
El ataque del taladrador de las meliáceas reduce el grado y así el valor monetario de las caobas jóvenes en viveros donde los cultivan para uso como árboles del paisaje, eso es, su principal uso en la Florida (Howard and Meerow 1993). Debido a que los ataques resultan en una reducción en el número y la longitud de troncos rectos y claros, el taladrador del brote de la caoba es una plaga importante de caobas, cedros, y otros árboles maderables meliáceos en las zonas tropicales. Los taladradores atacan un porcentaje más alto de los árboles de caoba que crecen en plantaciones que a aquellos que crecen entremezclados en bosques naturales, por ello este insecto ha sido un impedimento importante en el establecimiento de las plantaciones de caoba. Se necesitan urgentemente métodos para cultivar las caobas en plantaciones para así disminuir el impacto de cortarlos en bosques naturales (Lamb 1966; Newton et al. 1993; Mayhew and Newton 1998; Floyd and Hauxwell 2001).
Muchos autores han mencionado el daño a las semillas por el taladrador de las meliáceas, e.g., Monte (1933), Tillmanns (1964), Becker (1976), pero éste ha sido generalmente poco importante o en segundo lugar en importancia comparado con el daño a los brotes. Becker (1976) sugirió que la producción de semilla era suficiente para compensar las pérdidas por el taladrador de las meliáceas. Sin embargo, en un estudio en la Florida, el taladrador de las meliáceas atacó hasta 100% de las cápsulas de semilla por árbol de caoba antillana y consumió entre el 50% y 96% de las semillas por cápsula. Durante el mismo período, solamente un 14-22% de brotes nuevos en los árboles fue atacado. El impacto de este insecto en la regeneración se debe investigar más.
Manejo
La actividad de la investigación para desarrollar métodos de manejo ha sido mucho mayor para el taladrador de las meliáceas como plaga de los árboles maderables que de árboles ornamentales o de sombra (Lamb 1966; Grijpma 1974; Newton et al. 1993; Mayhew and Newton 1998; Floyd and Hauxwell 2001). En cualquier situación, este insecto es muy difícil de controlar, sobre todo porque, aunque algunos métodos reducen la población de la plaga considerablemente, hasta las poblaciones más pequeñas pueden causar daño significativo. De hecho, el daño más importante del insecto, la destrucción del brote terminal, es el resultado de una sola larva por árbol.
En la Florida, el taladrador de las meliáceas es en gran parte una plaga de la caoba antillana en viveros de macetas y viveros del campo en donde estos árboles nativos se tienen para el uso como árboles de sombra. Las caobas establecidas en el paisaje también son atacadas comúnmente por los taladradores de meliáceas, sobre todo en la primavera, pero el daño no afecta ni el crecimiento perceptiblemente ni la calidad estética de árboles maduros. Solamente se ataca un porcentaje de los brotes crecientes en un árbol, por ende el daño a las ramitas no es visible a distancia y el crecimiento de ramas durante el verano encubre el daño.
Control químico
Wylie (2001) hizo una revisión de la literatura sobre el control químico de Hypsipyla spp., concluyendo que después de más de ocho décadas de la investigación en 23 países tropicales todavía no existía ningún método de control químico confiable, económico y ambientalmente sano para prevenir daño económico por estos insectos. Él sugirió, sin embargo, que el control químico de estas plagas pudiera ser aplicable a las situaciones de viveros. Este puede ser el caso de la Florida, en donde el taladrador de las meliáceas ataca las ramitas sobre todo en la primavera, y las aplicaciones químicas se pueden concentrar así durante este período.
Como el primer instar de la larva puede alimentarse en los tejidos superficiales por un breve período antes de taladrar la ramita o la fruta (Ramírez Sánchez 1964), es teóricamente posible reducir poblaciones del taladrador de las meliáceas mediante aplicaciones tópicas de un plaguicida o de un 'antifeedant'. De hecho, aplicaciones tópicas repetidas del azadirachtin (extracto de la semilla del neem), un 'antifeedant' de insectos, a los árboles de caoba jóvenes durante el período principal del ataque de caoba del taladrador en la Florida (abril–mayo) redujeron la incidencia del daño (Howard 1995), no obstante un experimento similar después no fue conclusivo (Howard, inéditos). Algunos insecticidas de contacto que son eficaces contra otros taladradores de las ramitas han sido probados en el campo para reducir daño por el taladrador de meliáceas sin éxito. Un lavado de raíz con imidacloprid antes de la estación de primavera no protegió las caobas contra los taladradores (Howard, inéditos). Sin embargo, puesto que el imidacloprid es absorbido en diferentes tasas por diversas especies del árbol, debería evaluarse la eficacia de un lavado aplicado en la etapa temprana de la estación.
Control biológico
Cerca de 40 especies de insectos se han identificado como enemigos naturales del taladrador de las meliáceas en las Américas (Sands and Murphy 2001). Estas son, así como el taladrador de las meliáceas, nativas a la región; son también indudablemente de diferentes grados de importancia en la regulación de poblaciones de este insecto, pero su efecto no es suficiente para prevenir el daño económico. Aunque ha habido un cierto interés en las técnicas como el aumento de poblaciones de enemigos naturales, el control biológico del taladrador de las meliáceas no parece una opción prometedora (vea revisión por Sands and Murphy 2001). Esto se debe a que incluso las poblaciones más pequeñas pueden causar daño económico severo, según lo explicado previamente.
Silvicultura
Las caobas que crecen en bosques naturales lo hacen a menudo en bajas densidades y mezcladas con muchas otras especies. Bajo tales condiciones son menos probables a ser atacadas por los taladradores de las meliáceas. Este principio se ha aplicado en varias técnicas silviculturales con grados variables de éxito, y la investigación en esta área todavía sigue (Lamb 1966; Mayhew and Newton 1998; Hauxwell et al. 2001; Grogan et al. 2002). Se ha observado que en general las caobas que crecen en sombra tienden a ser menos susceptibles o escapan al ataque de la Hypsipyla spp., y las investigaciones recientes sobre el H. robusta indican que esta tendencia se debe a una diferencia fisiológica entre los árboles que crecen en sombra o en el ambiente abierto (Mahroof et al. 2000).
Mejoramiento de árboles
Al evaluar caobas y cedros de distintas procedencias, se han observado menos daños en algunas selecciones. La investigación para identificar las razas genéticas de estos árboles que sean resistentes o que puedan superar ataque del taladrador de las meliáceas ha progresado bien (Mayhew and Newton 1998; Watt et al. 2001).
Manejo integrado
Los participantes de un taller internacional sobre los taladradores Hypsipyla en 1996 concluyeron que las estrategias más prometedoras estaban relacionadas con la identificación y uso de genotipos resistentes, y el plantar árboles de caoba y cedro en plantíos mezclados a diferencia de plantíos puros y debajo de una canopia establecida. También se destacó que se debe promover el crecimiento vigoroso de árboles jóvenes por métodos culturales en el vivero y en plantaciones jóvenes. El control químico fue considerado como una herramienta para reducir temporalmente las poblaciones de los taladradores en áreas limitadas (Floyd 2001; Floyd and Hauxwell 2001; Speight 2001). Estas conclusiones se aplican sobre todo al manejo de las caobas y de otros árboles meliáceos cultivados para madera. El manejo integrado en los viveros en la Florida en donde la caoba se cultiva para árboles de sombra debe abarcar métodos como reducir poblaciones de la plaga durante la primavera y procedimientos de poda que promuevan la recuperación de los árboles que han sido atacados.
Agradecimientos
Agradecimientos a la Dra. Carrie Hauxwell, científica senior, Agency for Food and Fibre Sciences, Department of Primary Industries and Fisheries, Brisbane, Australia, por su revisión y sus comentarios sobre el manuscrito y a la Dra. Marianne Horak, especialista taxonómica en Lepidóptera, Australian National Insect Collection, CSIRO Entomology Canberra, Australia, por la información sobre el estado taxonómico actual de la Hypsipyla spp.
Referencias seleccionadas
Bauer GP. 1987. Swietenia macrophylla and Swietenia macrophylla X S.mahagoni development and growth: the nursery phase and the establishment phase in line planting in the Caribbean National Forest, Puerto Rico. M.S. Thesis. State University of New York, College of Environmental Science and Forestry, Syracuse, N.Y.
Becker VO. 1976. Microlepidopteros asociados con Carapa, Cedrela, y Swietenia en Costa Rica, pp. 75-101. In Whitemore JL [ed.], Studies on the shootborer, Hypsipyla grandella (Zeller), Lep.:Pyralidae, CATIE Misc. Publ. No. 1. CATIE, Turrialba, Costa Rica.
Cintron BB. 1990. Cedrela odorata L. Cedro hembra, Spanish cedar, pp. 250-257. In Burns RMH, Barbara H [ed.], Silvics of North America 2: Hardwoods. Agricultural Handbook 644. United States Department of Agriculture, Washington, DC.
Entwistle PF. 1967. The current situation on shoot, fruit and collar borers of the Meliaceae., Proceedings of the 9th British Commonwealth Forestry Conference. Commonwealth Forestry Institute, Oxford.
Floyd RB. 2001. General conclusions and research priorities. pp. 183-187. In Floyd RB, Hauxwell C (eds.), International Workshop on Hypsipyla shoot borers in Meliaceae, 20-23 August 1996. ACIAR Proceedings No. 97.
Floyd RB., Hauxwell C. [eds.] 2001. Hypsipyla shoot borers in Meliaceaae. Proceedings of an International Conference held at Kandy, Sri Lanka 20-23 August 1996. ACIAR Proceedings No. 97. Australian Centre for International Agricultural Research, Canberra, Australia.
Griffiths MW. 2001. The biology and ecology of Hypsipyla shoot borers. pp. 74-80. In Floyd RB, Hauxwell C (eds.), International Workshop on Hypsipyla shoot borers in Meliaceae, 20-23 August 1996. ACIAR Proceedings No. 97.
Grijpma P. 1970. Immunity of Toona ciliata M. Roem. var. australis (F. v. M.) DC. and Khaya ivorensis A. Chev. to attacks of Hypsipyla grandella Zeller in Turrialba. Turrialba 20: 85-93.
Grijpma P. 1974. Contributions to an integrated control programme of Hypsipyla grandella (Zeller) in Costa Rica. Landbouwhogeschool te Wageningen., Wageningen, Netherlands.
Grogan J, Barreto P, Veríssimo A. 2002. Mahogany in the Brazilian Amazon: Ecology and Perspectives on Management. Imazon, Belém, Pará, Brazil.
Hauxwell C, Mayhew JE, Newton AC. 2001. Silvicultural management of Hypsipyla spp. pp. 151-163. In Floyd RB, Hauxwell C, (eds.), International Workshop on Hypsipyla shoot borers in Meliaceae, 20-23 August 1996. ACIAR Proceedings No. 97.
Holsten EH. 1976. Life cycle of Hypsipyla grandella (Zeller). pp. 112-116. In Whitemore JL [ed.], Studies of the shootborer, Hypsipyla grandella (Zeller) Lep. Pyralidae, CATIE Misc. Publ. No. 1. CATIE, Turrialba, Costa Rica.
Horak M. 2001. Current status of the taxonomy of Hypsipyla Ragonot (Pyralidae: Phycitinae). pp. 151-163. In Floyd RB, Hauxwell C (eds.), International Workshop on Hypsipyla shoot borers in Meliaceae, 20-23 August 1996. ACIAR Proceedings No. 97.
Howard FW. 1991. Seasonal incidence of shoot infestation by mahogany shoot borer in Florida. Florida Entomologist 74: 150-151.
Howard FW. 1995. Reduction in damage to mahogany shoot borer and mahogany leaf miner by use of azadirachtin. Journal of Tropical Forest Science 7: 454-461.
Howard FW, Solis MA. 1989. The distribution, life history, and host plant relationships of mahogany webworm. Florida Entomologist 72: 469-477.
Howard FW, Meerow AW. 1993. Effect of mahogany shoot borer on growth of West Indies mahogany in Florida. Journal of Tropical Forest Science 6: 201-203.
Howard FW, Gilblin-Davis R. 1997. The seasonal abundance and feeding damage of Hypsipyla grandella (Lepidoptera: Pyralidae) in seed capsules of Swietenia mahagoni in Florida. Florida Entomologist 80: 35-41.
Lamb FB. 1966. Mahogany of Tropical America. Its Ecology and Management. University of Michigan Press, Ann Arbor.
Mahroof RM, Hauxwell C, Edirisinghe JP, Watt AD, Newton AC. 2000. Effects of artificial shade on attack by the mahogany shoot borer, Hypsipyla robusta (Moore). Agricultural and Forest Entomology 4: 283.
Mayhew JE, Newton AC. 1998. The Silviculture of Mahogany. CABI Publications, Wallingford, UK.
Monte O. 1933. Hypsipyla grandella Zeller, uma praga da silvicultura (Lep. Phycitidae). Revista de Entomología (Río de Janairo) 3: 281-285.
Newton AC, Baker P, Ramnarine S, Mesén JF, Leakey RRB. 1993. The mahogany shoot borer: prospects for control. Forest Ecology and Management 57: 301-328.
Pennington TD. 1981. A monograph of the neotropical Meliaceae. New York Botanical Gardens, New York.
Ramirez Sanchez J. 1964. Investigación preliminar sobre la biología, ecología y control de Hypsipyla grandella Zeller. Boletín del Instituto Forestal Latino-Americano, Mérida, Venezuela 16: 54-77.
Record SJ, Hess RW. 1943. Timbers of the New World. Yale University Press, New Haven, Connecticut.
Roovers M. 1971. Observaciones sobre el ciclo de vida de Hypsipyla grandella (Zeller) en Barinitas, Venezuela. Boletín del Instituto Forestal Latino-Americano de Investigación y Capacitación 38: 1-46.
Sands DPA, Murphy ST. 2001. Prospects for biological control of Hypsipyla spp. with insect agents. pp. 121-130. In Floyd RB, Hauxwell C (eds.), International Workshop on Hypsipyla shoot borers in Meliaceae, 20-23 August 1996. ACIAR Proceedings No. 97.
Solomon JD. 1995. Guide to insect borers of North American broadleaf trees and shrubs. Agriculture Handbook 706. US Department of Agriculture, Forest Service, Washington, DC.
Speight, M. R. 2001. Discussion summary: Integrated pest management of Hypsipyla spp. p. 179. In Floyd RB, Hauxwell C (eds.), International Workshop on Hypsipyla shoot borers in Meliaceae, 20-23 August 1996. ACIAR Proceedings No. 97.
Taveras R, Hilje L, Carballo M. 2004a. Development of Hypsipyla grandella (Zeller) (Lepidoptera: Pyralidae) in response to constant temperatures. Neotropical-Entomology 33: 1-6.
Taveras R, Hilje L, Hanson P, Mexzon R. 2004b. Population trends and damage patterns of Hypsipyla grandella (Lepidoptera: Pyralidae) in a mahogany stand, in Turrialba, Costa Rica. Agricultural and Forest Entomology 6: 89-98.
Tillmanns HJ. 1964. Apuntes bibliográficos sobre Hypsipyla grandella Zeller. Boletin del Instituto Forestal Latino-Americano, Mérida, Venezuela 14: 82-92.
Watt AD, Newton AC, Cornelius JP. 2001. Research in resistance of mahoganies to Hypsipyla species. pp. 89-96. In Floyd RB, Hauxwell C (eds.), International Workshop on Hypsipyla shoot borers in Meliaceae, 20-23 August 1996. ACIAR Proceedings No. 97.
Wylie FR. 2001. Control of Hypsipyla spp. shoot borers with chemical pesticides: a review. pp. 109-115. In Floyd. RB, Hauxwell C (eds.), International Workshop on Hypsipyla shoot borers in Meliaceae, 20-23 August 1996. ACIAR Proceedings No. 97: 109-115.