Introducción de la Marchitez del Laurel
El escarabajo ambrosia, Xyleborus glabratus, del laurel rojo y su hongo simbionte, Raffaelea lauricola (Rf), fueron introducidos durante el 2002 en Port Wentworth, Georgia, E.U., en embalajes de madera infestada procedentes de Asia (Mayfield and Thomas 2006). Este complejo insecto-hongo patógeno causa una enfermedad comúnmente conocida como la marchitez del laurel (ML) que afecta a los árboles de la familia Lauraceae y se transmite a través de las áreas naturales por el movimiento del escarabajo ambrosia del laurel rojo y también por movimientos antrópicos de productos maderables infestados (e.g., leña, madera para torneros, y madera para ahumados en barbacoa). En Florida, las plantas hospederas del complejo escarabajo ambrosia del laurel rojo - Rf incluyen al menos diez especies nativas de lauráceas leñosas (e.g., redbay [Persea borbonia] y el 'swampbay' [P. palustris]), así como también especies exóticas tales como el alcanfor (Cinnamomum camphora), aguacate (P. americana), y potencialmente el laurel de California (Umbellularia californica) (Campbell et al. 2017; Dreaden et al. 2016; Fraedrich 2008; Fraedrich et al. 2008; Fraedrich et al. 2011; Fraedrich et al. 2015; Hughes et al. 2012; Hughes et al. 2013; Hughes et al. 2014; Mayfield et al. 2013; Ploetz and Konkol 2013). A más tardar en febrero del 2010, los escarabajos ambrosia del laurel rojo fueron detectados en un área natural, 21 millas (33.7 km) al norte del área de producción de aguacates del sur de Florida (125 millas cuadradas; 324 km2) en el condado Miami-Dade (Thomas 2010; Ploetz, Peña et al. 2011). En esta misma área natural durante el 2011, fue documentada y confirmada la primera muerte de un árbol de 'swampbay' debido a la ML, y en 2012 la ML fue detectada en una arboleda comercial de aguacates (J. Crane, comunicación personal). Al contrario de las predicciones iniciales, las poblaciones de X. glabratus no se establecieron en las arboledas comerciales de aguacates. Sin embargo, la marchitez del laurel todavía es prevalente y continua su transmisión debido a una transferencia lateral inesperada de R. lauricola a escarabajos ambrosia nativos y exóticos, que ahora actúan como vectores secundarios de R. lauricola (Carrillo et al. 2014; Ploetz et al. 2017). Se ha demostrado que al menos dos especies de escarabajos ambrosia, Xyleborus volvulus y X. bispinatus, transmiten el agente patógeno de la marchitez del laurel a las arboledas de aguacate (Carrillo et al. 2014). Estos escarabajos ambrosia son más activos durante el atardecer (alrededor de las 4 PM- 8 PM y vuelan) generalmente a 10 pies (1.2 m) o menos del suelo (Menocal et al. 2018).
Actualmente, la ML ha sido detectada en 11 estados del sudeste de los E.U. que incluyen a Alabama, Arkansas, Florida, Georgia, Kentucky, Louisiana, Mississippi, North Carolina, South Carolina, Tennessee, y Texas (Figura 1; US Forest Service 2019), y en todos los 67 condados de Florida. La marchitez del laurel es ahora endémica en el área de producción de aguacates del condado Miami-Dade. Existe un gran riesgo de introducción de la ML en California, Méjico, Centro- y Suramérica mediante la transmisión natural del escarabajo ambrosia del laurel rojo hacia áreas de vegetación natural a través del movimiento de materiales maderables infestados (e.g., leña) (Crane et al. 2015; Ploetz, Smith et al. 2011).
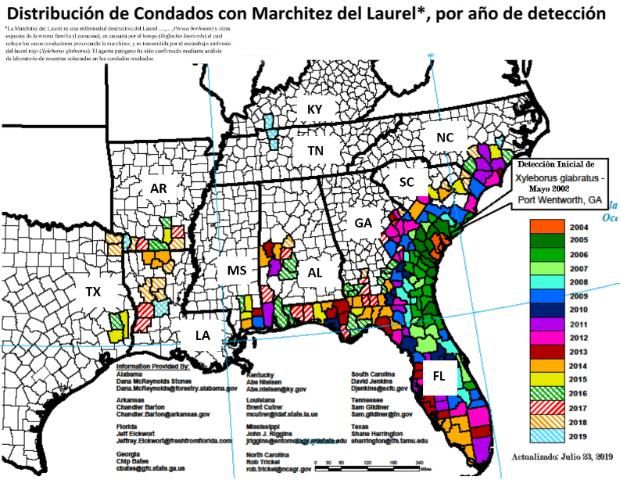
Credit: US Forest Service
En una prueba de cultivo controlado en macetas, la susceptibilidad a la ML de 24 variedades de aguacate con dotaciones genéticas variadas fue probada y aquellas variedades con dotación genética Guatemalteca X Mejicana (e.g., 'Hass', 'Winter Mexican') fueron menos afectados por la inoculación de la ML que otras variedades con dotaciones Guatemalteca X Antillano (e.g., 'Miguel'), las cuales a su vez fueron menos afectadas que las variedades Antillanas (e.g., 'Simmonds' y 'Donnie') (Ploetz, Pérez-Martínez et al. 2011). Esto sugiere que existe variabilidad en la rapidez conque los síntomas de la ML progresan y que la misma tiene una base genética. Además, la severidad de los síntomas estuvo correlacionada positivamente con el tamaño de las plantas; las plantas más grandes reaccionan más rápidamente a la infección del agente patógeno que las plantas más pequeñas.
En las arboledas comerciales, se ha documentado que los árboles adultos de 32 variedades de aguacates con diferentes dotaciones genéticas perecen debido a la ML (Tabla 1) (A. Palmateer, R. Gazis, y J. Crane, observaciones personales). Hasta el presente, no se ha descubierto que en alguna variedad los árboles adultos sean tolerantes a la ML. Recientemente, estudios en invernaderos han mostrado que la tasa de progresión de la ML (i.e., la velocidad conque los síntomas se desarrollan) está más relacionada con el injerto que con el portainjerto, pero que el portainjerto tiene alguna influencia (B. Schaffer, comunicación personal). Hasta este momento no se ha confirmado la tolerancia de injerto o portainjerto alguno, pero la investigación continúa para tratar de identificar injertos, portainjertos y sus combinaciones que sean tolerantes a la ML.
En arboledas de aguacates adultos, la enfermedad ML se disemina por injertos de raíces entre árboles adyacentes y mediante las infestaciones de escarabajos ambrosia (EA). Por la vía de injertos de raíces, el agente patógeno se desplaza con una tasa de tres a seis nuevos árboles por mes; esto puede traer como consecuencia la pérdida de 90 o más árboles en un período de seis meses (Crane et al. 2016; Ploetz et al. 2017). Los síntomas visibles de la enfermedad marchitez del laurel comienzan por la marchitez de las hojas todavía verdes, típicamente en una sección del árbol (Figura 2). Las perforaciones de los EA producen tubitos de un exudado blanquecino que pueden ser evidentes y la albura frecuentemente presenta estrías negruscas-azulosas. A medida que la enfermedad progresa, las hojas se secan, tornan carmelitas, pero permanecen unidas a las ramas (hasta 12 meses) y la muerte regresiva invade más secciones del árbol. En ocasiones, ocurre una caída grande de hojas durante los primeros estadíos de la enfermedad, pero subsecuentemente ocurre la muerte regresiva y la muerte del árbol comienza (Figura 3). En ambos casos el árbol muere eventualmente, aunque a veces si no se remueve el árbol o tocón puede rebrotar del tocón o raíces grandes (Figura 4). Existen reportes contradictorios respecto a la capacidad que tienen los árboles infectados con la ML a recuperarse después de ser cortados en tocones. (altura de ~4 p; ~1.2 m). Se ha reportado que algunos árboles vuelven a desarrollar una copa y parecen estar libres de la enfermedad, pero este nuevo crecimiento sufre muerte regresiva repetidamente hasta que el árbol finalmente muere. También se ha reportado que los tocones vuelven a desarrollar sus copas y vuelven a producir frutos después de dos a tres años. No sabemos cuán frequentemente ocurre el reverdecimiento y la reanudación de la producción, pero este aspecto está siendo evaluado.

Credit: J. H. Crane, UF/IFAS

Credit: J. H. Crane, UF/IFAS

Credit: J. H. Crane, UF/IFAS
Hallazgos de la Investigación Relacionada con las Estrategias de Control Vigentes
- La marchitez del laurel es muy virulenta pues árboles inoculados con una cantidad tan pequeña como 39 unidades formadoras de colonias (UFC) pueden morir en estado adulto (R.C. Ploetz, datos inéditos). Mientras mayor sea el número UFC, más rápidamente comienza la progresión de la enfermedad. El agente patógeno se mueve rápidamente a nuevos sitios dentro del xilema provocando que los mecanismos de defensa del árbol (producción de tílides, i.e., estructuras que bloquean los vasos conductores, y gomas) rápidamente bloqueen el tejido transportador del agua y por lo tanto el árbol muere (Inch and Ploetz 2012; Inch et al. 2012).
- Recomendaciones previas, basadas en investigaciones, sugirieron que las infusiones profilácticas (similares a los sistemas de perfusión intravenosa) con el fungicida sistémico propioconazol (Tilt®) podían proteger a los árboles de aguacate de la ML por un período de 12 a 18 meses (Crane et al. 2016; Ploetz et al. 2011). Sin embargo, la infusión del fungicida propioconazol es muy costosa y puede ocasionar daños físicos a los árboles debido a las inyecciones repetidas (Evans et al. 2015).
Al contrario, las inyecciones profilácticas con Tilt® son mucho menos costosas y se ha demostrado que previenen los brotes de ML en las arboledas comerciales de aguacate. El movimiento sistémico del fungicida a través del árbol toma de siete a ocho meses, y la protección que brinda a la ML ha sido reportada en un rango de 12-14 meses, dependiendo de la tasa de fungicida, el tamaño del árbol, estado de la arboleda en el momento de infección con la ML, y la historia de la arboleda con respecto a esta enfermedad (Brooks Tropical, comunicación personal).
3. Varios insecticidas por contacto convencionales han mostrado ser eficaces en el control de los escarabajos ambrosia incluyen a Malathion (malatión), Danitol® (fenpropatrina), Agri-Mek®SC (abamectina), Talstar®S (bifentrina), y Hero® (cipermetrina + bifentrina; solo en árboles sin frutos) (Carrillo et al. 2013; Peña et al. 2011). No obstante, estos insecticidas son efectivos sólo cuando el escarabajo ambrosia (EA) está fuera del árbol, y EA pasa la mayor parte de su ciclo de vida dentro del árbol. Por estas razones, los insecticidas convencionales sólo se recomiendan para suprimir las poblaciones activas de escarabajos ambrosia después de remover y convertir en serrín los árboles infestados, infectados o ambos.
4. Además, se ha demostrado que varios hongos entomopatógenos (Beauveria bassiana) pueden infectar a los EA, incluyendo a los estadíos inmaduros que se desarrollan dentro de los árboles (Carrillo et al. 2015; Avery et al. 2018). Pero, después de 8 meses de haber aplicado formulaciones comerciales de hongos entomopatogénos (e.g., BotaniGard y Mycotrol) a las superficies de los árboles, se ha documentado la infección dentro de los mismos. Además, debido al alto costo de las formulaciones comerciales de hongos entomopatógenos, las aplicaciones de estos hongos a nivel de arboledas sólo se recomiendan durante los meses de actividad intensa del EA (a finales del invierno y principios de la primavera).
5. En lugares donde los niveles de luz solar son significativamente más altos, la actividad del EA está significativamente reducida, e.g., arboledas recién plantadas, áreas donde los árboles se han convertidos en tocones (cortados a una altura de 4 p [1.2 m]), y áreas de arboledas donde recientemente se han injertado los árboles. La diferencia en actividad del EA se evidencia cuando estas áreas se comparan con arboledas con copas muy densas y por lo tanto muy sombreadas (Figura 5; D. Carrillo y J. Crane, datos inéditos). Por lo tanto, se recomienda la implementación o restablecimiento de un programa de poda para mejorar la penetración de la luz solar dentro de las arboledas para reducir la actividad de los EA y nuevos brotes de ML. Alternativamente, el rejuvenecimiento o poda de injerto de los árboles adultos puede ser una opción para restablecer condiciones de alta iluminación dentro de las arboledas (descrita en detalle posteriormente).

Credit: J. H. Crane, UF/IFAS
Opciones Actuales de Control y Recomendaciones de Mitigación
General
- Para mantener los árboles saludables, se deben optimizar las prácticas de fertilización e irrigación, así como las medidas para controlar la pudrición por Phytophthora y otras enfermedades. Los árboles saludables son menos susceptibles al ataque de los EA que los árboles estresados con deficiencias nutricionales (J. Crane, comunicación personal). Cualquier estrés (e.g., inundación, sequía, congelación, otros agentes patógenos etc.) causa que los árboles de aguacates sean más atractivos para los EA.
- Monitorear las arboledas frecuentemente para detectar los árboles con los síntomas tempranos de la ML (i.e., marchitez de las hojas verdes). La importancia de la detección temprana no debe ser subestimada debido a la rápida dispersión del hongo patógeno entre árboles adyacentes mediante injerto de raíces.
- Remover los árboles afectados por la ML inmediatamente: desraizar y triturar/aserrar el árbol completo (raíces, troncos, ramas, etc.). Es imperativo que los árboles afectados por la ML sean desraizados para reducir la transmisión del hongo patógeno hacia los árboles adyacentes.
Inyecciones Profilácticas con Fungicidas
- De manera profiláctica, inyecte todos los árboles en la arboleda con propiconazol (Tilt®) antes de que ocurra un brote de Marchitez del Laurel. Si las aplicaciones no se pueden realizar a todos los árboles, remueva los árboles sintomáticos como se indicó anteriormente e inyecte todos los otros árboles que lucen saludables. Algunos árboles que aparentan estar saludables podrían aún morir debido a la dispersión previa del agente patógeno antes de las inyecciones. Estos árboles deber removerse lo más rápido que sea posible. Los árboles necesitan recibir inyecciones repetidas con un intervalo de 12 a 24 meses, dependiendo de la tasa de Tilt® usada, actividad del EA (i.e., iniciando nuevas infestaciones), y la presión existente de la ML (i.e., medida por cuántos nuevos brotes de ML ocurren) (Brooks Tropicals, comunicación personal).
- Cuando usen Tilt®, los cosecheros deben tener la etiqueta Section 18 'special local needs label (SLN)'; comuníquese con Jef Wasielewski, el agente de Producción Comercial de Frutos de UF/IFAS en la oficina de Extensión (305-248-3311, ext. 227; jwasielewski@ufl.edu).
Control del Escarabajo Ambrosia
- Rocie dos veces la madera triturada/serrín con un insecticida de contacto. Los insecticidas inscritos para los aguacates incluyen a Malathion (malatión), Danitol® (fenpropatrina), Agri-Mek®SC (abamectina), Talstar®S (bifentrina), y Hero® (sólo en árboles sin frutos), Botanigard® y Mycotrol® (Beauveria bassiana).
- Realice dos aplicaciones, con un insecticida de contacto inscrito, dirigidas hacia los troncos y ramas principales (hasta aproximadamente 10 p [3 m]) con un intervalo de 14 días a todos los árboles saludables que se encuentran en el 1 acre (0.4 ha) que rodea al árbol eliminado debido a su afectación por la ML.
- Durante finales del invierno y comienzo de la primavera, cuando las poblaciones del EA aumentan, realice dos aplicaciones de micoinsecticidas, Botanigard®ES o Mycotrol® (Beauveria bassiana), a toda la arboleda para suprimir las poblaciones del EA.
Prácticas Culturales y Mitigación
- Mantenga un régimen de poda para incrementar la penetración de la luz solar y las horas de alta iluminación en las arboledas de aguacates lo cual ayudará a suprimir la actividad de los escarabajos ambrosia. Esto puede realizarse con equipos mecánicos de poda (i.e., podadoras de discos) o mediante poda manual selectiva. Otra opción es convertir los árboles en tocones de aproximadamente 4 p (rejuvenecimiento) y después injertarlos con nuevas variedades.
- Rejuvenezca los árboles muy viejos y grandes que han perdido la mayor parte de su producción en las partes bajas de las copa. Para lograrlo, pódelos a una altura (tocón) de 4 a 8 pies. Pinte con lechada las ramas principales para prevenir las quemaduras por el sol en los troncos y ramas principales. Los árboles comenzarán a reverdecer y restablecer las copas dentro de unos cuantos meses y comenzarán a producir frutos aproximadamente en un período de 3 años. De forma alternativa, el nuevo crecimiento de estos árboles puede injertarse con otras variedades que sean más rentables, productivas o ambas. Nuevamente, estos árboles injertados con nuevas variedades pueden empezar su producción después de aproximadamente 3 años.
- Resiembre los árboles de aguacate perdidos por la ML para incrementar la producción futura y mantener su viabilidad económica (Evans et al. 2010; Mosquera et al. 2015). El movimiento del agente patógeno de la ML debido a injertos de raíces no es un problema en los árboles jóvenes porque toma varios años la formación de este tipo de injerto, además los EA no prefieren a los árboles jóvenes como hospederos, y la alta exposición a la luz en el área que rodea a estos árboles suprime la actividad del EA.
Comentarios Finales
El control del complejo agente patógeno ML - EA es difícil debido a la posibilidad de que ocurra una transmisión rápida por injertos de raíces, por nuevas infestaciones de ML debido al movimiento del EA, y a las dificultades y costos de las tácticas de control existentes. Las investigaciones en curso tienen como objetivo lograr un conocimiento más profundo de la biología del agente patógeno de la ML y el EA capaz de transmitirlo, de la epidemiología (dinámica de la dispersión de la enfermedad), y desarrollar métodos de control y tácticas de mitigación más eficaces. Las recomendaciones de control serán revisadas tan pronto se conozca información adicional.
Agradecimientos
Los autores agradecen el apoyo de las siguientes entidades: beca 'USDA- NIFA grant 2015-51181-24257: Laurel Alt of Avocado: Management of an Unusual and Lethal Disease'; Instituto de Ciencias Alimentarias y Agrícolas, University of Florida; Florida Avocado Administrative Committee; Extensión UF/IFAS Extension Miami-Dade County; y al Departamento de Agricultura y Servicios al Consumidor de Florida.
Bibliografía Citada
Avery, P. B., V. Bojorque, C. Gámez, R. E. Duncan, D. Carrillo, and R. D. Cave. 2018. "Spore Acquisition and Survival of Ambrosia Beetles Associated with the Laurel Wilt Pathogen in Avocados after Exposure to Entomopathogenic Fungi." Insects 9 (2): 49. http://dx.doi.org/10.3390/ insects9020049
Campbell, A. S., R. C. Ploetz, and J. A. Rollins. 2017. "Comparing Avocado, Swamp Bay, and Camphor Tree as Hosts of Raffaelea lauricola Using a Green Fluorescent Protein (GFP)-Labeled Strain of the Pathogen." Phytopathology 107:70–74.
Carrillo, D., J. H. Crane, and J. E. Peña. 2013. "Potential of Contact Insecticides to Control Xyleborus glabratus (ColWioptera: Curculionidae), a Vector of Laurel Wilt Disease in Avocados." J. Econ. Entomol. 106 (6): 2286–2295.
Carrillo, D., R. E. Duncan, and J. E. Peña. 2012. "Ambrosia Beetles (Coleoptera: Curculionidae: Scolytinae) That Breed in Avocado Wood in Florida." The Fla. Entomologist 95 (3): 573–579.
Carrillo, D., R. E. Duncan, J. N. Ploetz, A. F. Campbell, R. C. Ploetz, and J. E. Peña. 2014. "Lateral Transfer of a Phytopathogenic Symbiont among Native and Exotic Ambrosia Beetles." Plant Pathology 63:54–62.
Carrillo, D., C. A. Dunlap, P. B. Avery, J. Navarrete, R. E. Duncan, M. A. Jackson, R. W. Behle, R. D. Cave, J. Crane, A. P. Rooney, and J. E. Peña. 2015. "Entomopathogenic Fungi as Biological Control Agents for the Vector of the Laurel Wilt Disease, the Redbay Ambrosia Beetle, Xyleborus glabratus (Coleoptera: Curculionidae)." Biological Control 81:44–50.
Crane, J. H., E. A. Evans, D. Carrillo, R. C. Ploetz, and A. J. Palmateer. 2015. "The Potential for Laurel Wilt to Threaten Avocado Production Is Real." ACTAS, Proceedings of the VIII Congreso Mundial de la Palta, Lima, Peru. 13–18 Sept. 2015.
Crane, J. H., R. C. Ploetz, T. White, G. C. Krogstad, T. Prosser, J. Konkol, and R. Ademan. 2015. "Efficacy of Three Microinfused Fungicides to Control Laurel Wilt on Avocado in Martin and Brevard Counties." Proc. Fla. State Hort. Soc. 128:58–60.
Dreaden, T. J., A. S. Campbell, C. A. Gonzalez-Benecke, R. C. Ploetz, and J. A. Smith. 2016. "Response of Swamp Bay, Persea palustris, and Redbay, P. bornbonia, to Raffaelea spp. Isolated from Xyleborus glabratus." Forest Pathology 2017 (47): e12288. https://doi.org/10.1111/efp.12288
Evans, E. A., J. Crane, A. Hodges, and J. L. Osborne. 2010. "Potential Economic Impact of Laurel Wilt Disease on the Florida Avocado Industry." HortTechnology 20 (1): 234–238.
Evans, E. A., J. H. Crane, R. C. Ploetz, and F. H. Ballen. 2015. "Cost-Benefit Analysis of Area-wide Management of Laurel Wilt Disease in Florida Commercial Avocado Production Area." Proc. VIII Congreso Mundial de la Palta (Colombia; in Spanish). 467–470.
Fraedrich, S. W. 2008. "California Laurel Is Susceptible to Laurel Wilt Caused by Raffaelea lauricola." Plant Dis. 92:1469.
Fraedrich, S. W., T. C. Harrington, C. A. Bates, J. Johnson, L. S. Reid, G. S. Best, T. D. Leininger, and T. S. Hawkins. 2011. "Susceptibility to Laurel Wilt and Disease Incidence in Two Rare Plant Species, Pondberry and Pondspice." Plant. Dis. 95:1056–1062.
Fraedrich, S. W., T. C. Harrington, and G. S. Best. 2015. "Xyleborus glabratus Attacks and Systemic Colonization by Raffaelea lauricola Associated with Dieback of Cinnamomum camphora in the Southeastern United States." For. Path. 45:60–70.
Fraedrich, S. W., T. C. Harrington, R. J. Rabaglia, M. D. Ulyshen, A. E. Mayfield, III, J. L. Hanula, J. M. Eickwort, and D. R. Miller. 2008. "A Fungal Symbiont of the Redbay Ambrosia Beetle Causes a Lethal Wilt in Redbay and Other Lauraceae in the Southeastern United States." Plant Dis. 92:215–224.
Hughes, M. A., A. Black, and J. A. Smith. 2014. "First Report of Laurel Wilt Caused by Raffaelea lauricola on Bay Laurel (Laurus noblis) in the United States." Plant Dis. 98:1159.
Hughes, M. A., G. Brar, R. C. Ploetz, and J. A. Smith. 2013. "Field and Growth Chamber Inoculations Demonstrate Persea indica a Newly Recognized Host of the Laurel Wilt Pathogen, Raffaelea lauricola." Plant Health Progress 14 (1). https://doi.org/10.1094/PHP-2013-0814-02-BR
Hughes, M. A., K. Shin, J. Eickwort, and J. A. Smith. 2012. "First Report of Laurel Wilt Disease Caused by Raffaelea lauricola on Silk Bay in Florida." Disease Notes 96:910.
Inch, S. E., and R. C. Ploetz. 2012. "Impact of Laurel Wilt, Caused by Raffaelea lauricola, on Xylem Function in Avocado, Persea americana." For. Path. 42:239–245.
Inch, S., R. Ploetz, B. Held, and R. Blanchette. 2012. "Histological and Anatomical Responses in Avocado, Persea americana, Induced by the Vascular Wilt Pathogen, Raffaelea lauricola." Botany 90:627–635.
Mayfield, A. E., III, M. MacKenzie, P. G. Cannon, S. W. Oak, S. Horn, J. Hwang, and P. E. Kendra. 2013. "Suitability of California Bay Laurel and Other Species as Hosts for the Non-native Redbay Ambrosia Beetle and Granulate Ambrosia Beetle." Agric. and Forest Entomology 15:227–235.
Mayfield, A. E., III, and M. C. Thomas. 2006. "The Redbay Ambrosia Beetle, Xyleborus glabratus Eichhoff (Scolytinae: Curculionidae)." DACS-P-01651. Florida Department of Agriculture and Consumer Services, Division of Plant Industry. https://www.freshfromflorida.com/content/ download/66299/1600379/PEST_ALERT_-_Xyleborus_gla- bratus_-_Redbay_Ambrosia_Beetle.pdf
Menocal, O., P. E. Kendra, W. S. Montgomery, J. H. Crane, and D. Carrillo. 2018. "Vertical Distribution and Daily Flight Periodicity of Ambrosia Beetles (Coleoptera: Curculionidae) in Florida Avocado Orchards Affected by Laurel Wilt." J. Econ. Entomology 111 (3): 1190–1196.
Mosquera, M., E. A. Edwards, and R. Ploetz. 2015. "Assessing the Profitability of Avocado Production in South Florida in the Presence of Laurel Wilt." Theoretical Economics Letters 5:343–356.
Peña, J. E., J. H. Crane, J. L. Capinera, R. E. Duncan, P. E. Kendra, R. C. Ploetz, S. McLean, G. Brar, M. C. Thomas, and R. D. Cave. 2011. "Chemical Control of the Redbay Ambrosia Beetle, Xyleborus glabratus, and Other Scolytinae (Coleoptera: Curculionidae)." Fla. Entomol. 94 (4): 882–896.
Ploetz, R. C., and J. Konkol. 2013. "First Report of Gulf Licaria, Licaria trianda, as a Suspect of Laurel Wilt" Plant Dis. 97:1248.
Ploetz, R. C., J. L. Konkol, J. M. Pérez-Martínez, and R. Fernandez. 2017. "Management of Laurel Wilt of Avocado, Caused by Raffaelea lauricola." Eur. J. Plant Pathol. 149:133–143. https://doi.org/10.1007/s10658-017-1173-1
Ploetz, R. C., J. E. Peña, J. A. Smith, T. J. Dreaden, J. H. Crane, T. Schubert, and W. Dixon. 2011. "Laurel Wilt, Caused by Raffaelea lauricola, Is Confirmed in Miami-Dade County, Center of Florida's Commercial Avocado Production." Disease Notes 95 (12): 1589.
Ploetz, R. C., J. M. Pérez-Martínez, J. A. Smith, M. Hughes, T. J. Dreaden, S. A. Inch, and Y. Fu. 2011. "Responses of Avocado to Laurel Wilt, Caused by Raffaelea lauricola." Plant Pathology 61 (4): 801–808. https://doi. org/10.1111/j.1365-3059.2011.02564.x
Ploetz, R. C., J. A. Smith, S. A. Inch, J. E. Peña, E. A. Evans, J. H. Crane, P. Kendra, J. Hulcr, L. Stelinski, and R. Schnell. 2011. "Laurel Wilt: A Global Threat to Avocado Production." Proc. VII World Avocado Congress, Cairns, Australia.
Thomas, M. C. 2010. "Entomology Specimen Report." E2020-1101-1. Gainesville, FL: Fla. Dept. Agric. and Consumer Services, Div. of Plant Industry.
US Forest Service. 2019. "Distribution of Counties with Laurel Wilt Disease by Year of Initial Detection." https://www.fs.usda.gov/Internet/FSE_DOCUMENTS/fseprd571973.pdf