Introducción
El picudo del botón del hibisco (Anthonomus testaceosquamosus Linell, Coleoptera: Curculionidae) es una plaga del hibisco (Hibiscus rosa-sinensis L., Malvales: Malvaceae), originaria del noroeste de México y sur de Texas, que fue visto en Florida por primera vez en mayo del 2017 (Skelley y Osborne 2018). El incremento de las poblaciones del picudo entre 2019 y 2020 impactó negativamente la industria del hibisco en el sur de Florida durante el periodo de empaque en la primavera, lo que resultó en grandes pérdidas económicas. Florida lidera la producción de hibisco a nivel nacional, donde la mayoría de la producción en viveros ocurre en el sur del estado. Aproximadamente entre el 20 y el 25% de las plantas vendidas en el condado de Miami-Dade son hibiscos, donde el valor del mercado de plantas ornamentales fue de 697 millones (precio en el vivero) en 2017 (Departamento de Agricultura de los Estados Unidos, 2017). El picudo del botón del hibisco es una plaga regulada por la División de Industria Vegetal del Departamento de Agricultura y Servicios al Consumidor (FDACS-DPI, por sus siglas en inglés). De acuerdo con esta designación, cualquier vivero que sea identificado con la presencia de la plaga debe firmar y seguir un acuerdo de cumplimiento con el FDACS-DPI para reducir las probabilidades de dispersión del picudo. El propósito de este documento es proveer información acerca de esta importante plaga a productores de viveros y al público interesado.
Identificación
El picudo del botón del hibisco (Orden Coleoptera) pertenece a la familia de los picudos (Curculionidae) y a su vez pertenece al grupo de especies conocido como Anthonomus squamosus de la tribu Anthonomini. Este grupo de especies se caracteriza por tener insectos predominantemente cubiertos de escamas (Clark et al. 2019) (Figura 1). La longitud del cuerpo del adulto está entre 2,5 y 2,7 mm y el pico es de aproximadamente 1 mm de largo.

Credit: Daniel Carrillo, UF/IFAS TREC
Las hembras se pueden distinguir de los machos mediante dos características, una es la protibia (el cuarto segmento del primer par de patas) y otra es el abdomen. En la protibia las hembras tienen un uncus apical y subapical, prominencia interior-marginal (mucron) (estructura en forma de espuela del lado interno de la tibia) (Figura 2a), que está ausente en los machos (Figura 2b). Adicionalmente, la parte posterior del quinto tergito abdominal (margen del quinto segmento abdominal) es recto en las hembras (Figura 3a, derecha) y curvo en los machos (Figura 3b, izquierda). La validez de estos caracteres fue confirmada mediante la disección de la genitalia de los picudos (Figura 4).
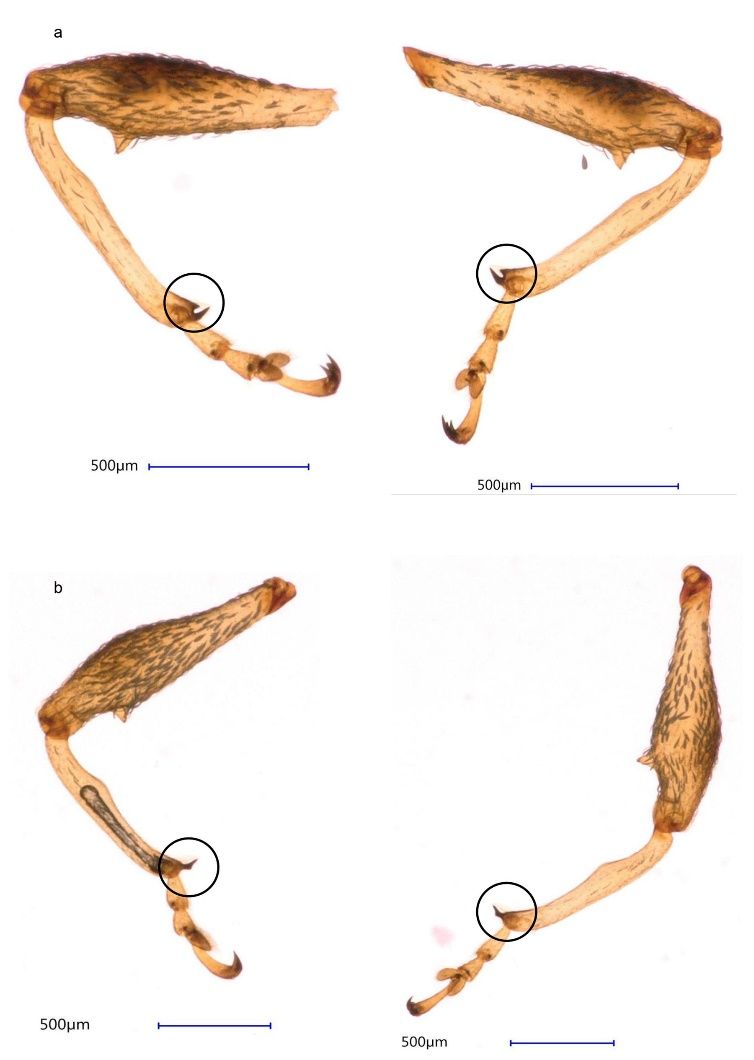
Credit: Daniel Carrillo, UF/IFAS TREC

Credit: Daniel Carrillo, UF/IFAS TREC
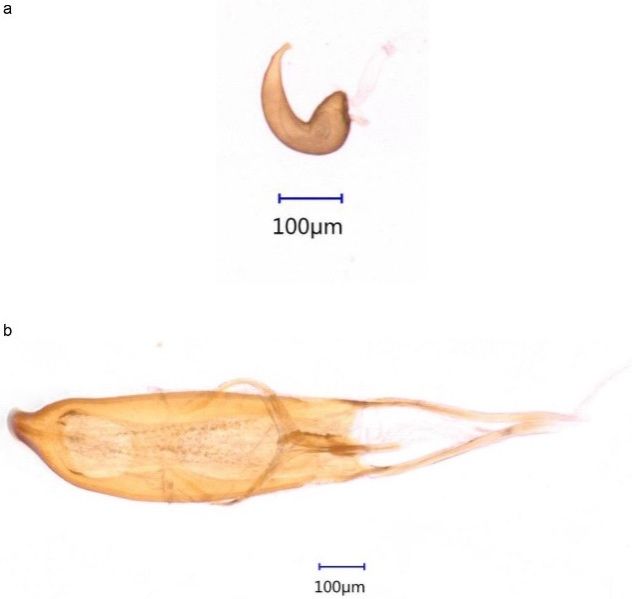
Credit: Daniel Carrillo, UF/IFAS TREC
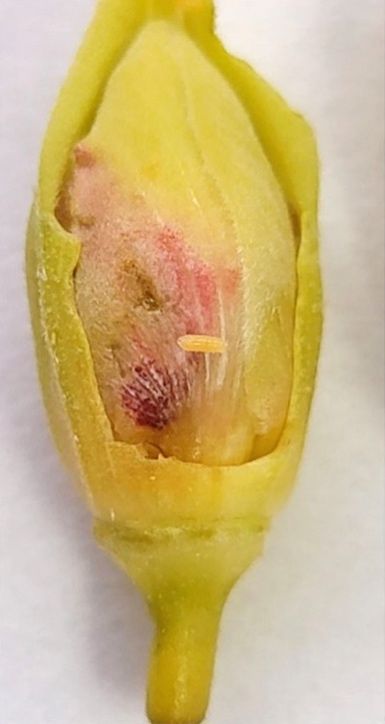
Los huevos son blancos cuando están recién depositados y se tornan amarillos al madurar (Figura 5). Las larvas del picudo del hibisco son de un color entre transparente y amarillo, tienen una cápsula cefálica bien definida y están desprovistas de patas torácicas (Figura 6). El tamaño de las larvas varía con el tamaño de los botones florales en donde se encuentran. En general, los botones florales grandes contienen larvas de mayor tamaño.

Credit: Juleysy Rodríguez y Yisell Velázquez Hernández, UF/IFAS TREC
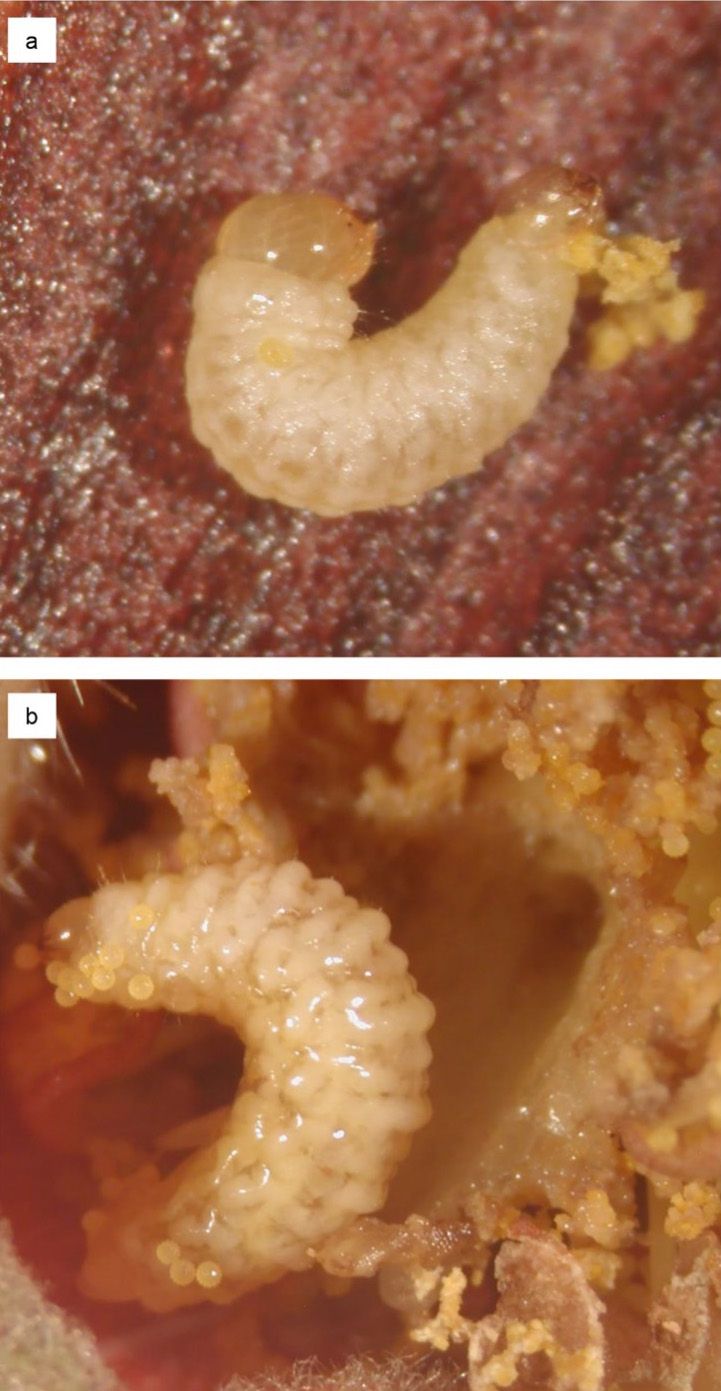
Credit: Juleysy Rodríguez y Yisell Velázquez Hernández, UF/IFAS TREC
Rango de hospederos y daño
Los picudos pertenecientes al grupo de Anthonomus squamosus están asociados con especies de plantas de las familias Asteraceae o Malvaceae. El picudo del botón del hibisco, A. testaceosquamosus ha sido asociado con múltiples especies de plantas, todas dentro de la familia Malvaceae (Tabla 1).
Tabla 1. Especies de plantas en las cuales el picudo del botón del hibisco Anthonomus testaceosquamosus Linell ha sido encontrado (Clark et al. 2019).
Los adultos del picudo se alimentan principalmente de botones florales, tallos y en menor medida de hojas del hibisco. Las hembras ovipositan en los botones florales y las larvas se desarrollan en el interior del botón, causando la caída de este antes de la floración. Los síntomas incluyen perforaciones en los tallos y botones a punto de abrir (Figura 7), y caída severa de botones bajo condiciones de alta densidad de la plaga. El daño producido por la alimentación en las hojas no es muy llamativo. En viveros del sur de Florida, las variedades rosadas y amarillas parecen ser más susceptibles al picudo que las rojas y otras variedades (Tabla 2). La variedad rosada ‘Painted Lady’ y la variedad amarilla ‘Sunny Yellow’ son reportadas como las variedades más susceptibles. La variedad roja ‘President Red’ es reportada como la más resistente.
Tabla 2. Variedades de hibisco cultivadas en Florida que han sido encontradas infestadas por el picudo del botón del hibisco (Anthonomus testaceosquamosus).
En Florida, otra especie del grupo Anthonomus squamosus, Anthonomus rubricosus, ha sido reportada infestando algodón y plantas de hibisco (Clark et al. 2019; Loiácono et al. 2003). Sin embargo, no existen reportes recientes de su establecimiento en plantas de hibisco en Florida. Este picudo es similar en tamaño al picudo del hibisco, pero es de color café. El genero Anthonomus incluye varias especies de gran importancia agrícola, como el picudo del algodonero, Anthonomus grandis. Las plagas del género Anthonomus más importantes desde el punto de vista económico en Florida son el picudo del chile Anthonomus eugenii y el picudo de la acerola Anthonomus macromalus. El picudo del chile ataca plantas de la familia Solanaceae, particularmente chiles (Capsicum spp.) (Capinera 2002), mientras que el picudo de la acerola ataca la cereza de Barbados (Malpighia glabra, Familia: Malpighiaceae) (Hunsberger y Peña 1998).

Credit: Juleysy Rodríguez y Yisell Velázquez Hernández, UF/IFAS TREC
La caída de los botones también puede ser causada por la mosquita de la flor (Contarinia maculipennis, Diptera: Cecidomyiidae), que puede ser confundida con daño por parte del picudo del botón del hibisco (Mannion et al. 2006). Ambas plagas pueden infestar la misma planta de hibisco; sin embargo, rara vez se encuentran en el mismo botón floral. Botones infestados con la mosquita de la flor tienen internamente múltiples larvas de mosca de color entre blanco y amarillo que saltan cuando son molestadas. Las larvas de la mosquita de la flor no tienen una cabeza distinguible y patas, y necesitan abandonar el botón para empupar en el suelo, mientras que la larva del picudo del hibisco tiene cabeza y empupa dentro del botón floral (Figuras 8 y 9).

Credit: Juleysy Rodríguez y Yisell Velázquez Hernández, UF/IFAS TREC
Credit: Juleysy Rodríguez y Yisell Velázquez Hernández, UF/IFAS TREC
Biología
Las hembras del picudo del botón del hibisco ovipositan entre 3 y 5 huevos en un solo botón floral y cerca de las anteras (Figura 4). Una vez que las larvas eclosionan se alimentan de polen y permanecen dentro del botón floral hasta alcanzar el estado adulto. Debido a una alta incidencia de canibalismo en el estado de larva, no todos los huevos depositados en un botón llegan al estado adulto; sin embargo, varios adultos pueden emerger de un solo botón floral. A una temperatura de 26,7 °C (8 0°F), los huevos pueden emerger entre 2 y 3 días. El estado de larva tiene tres instares y puede durar, en promedio, 10 días. El estado de pupa dura entre 2,9 a 4,2 días (Figura 10). El desarrollo entre el estado de huevo y el adulto puede tomar entre 12,8 y 15,3 días, en el cual se ha observado una sobrevivencia de hasta el 90%. La longevidad de los adultos tiene un rango entre 13 y 169 días, y los machos viven por más tiempo que las hembras. Cuando los adultos son alimentados solamente usando polen pueden sobrevivir hasta 52 días. Los adultos sobreviven un promedio de 28 días sin acceso a alimento, pero con acceso a agua, y pueden sobrevivir 16 días sin alimento y sin agua. La proporción sexual es de 1:1 hembras por machos (Revynthi et al. 2022).
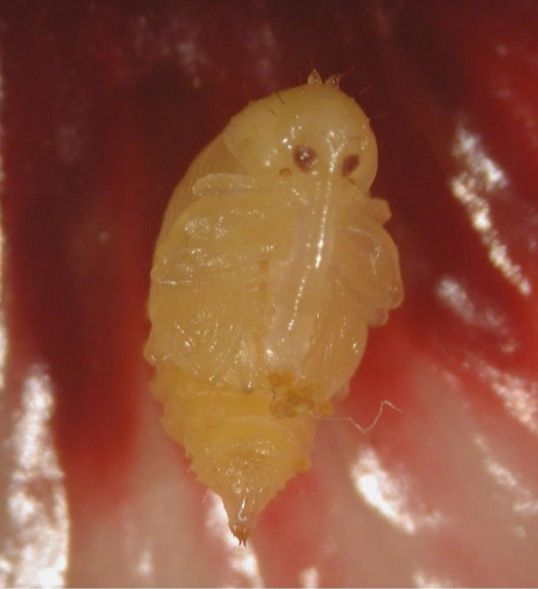
Credit: Juleysy Rodríguez y Yisell Velázquez Hernández, UF/IFAS TREC
Temperaturas extremas ya sean bajas o altas parecen ser perjudiciales para el desarrollo de las larvas del picudo. En experimentos de laboratorio en la Universidad de Florida, a 10 °C (50 °F) no hubo eclosión de huevos, mientras que a 15 °C (59 °F) hubo eclosión 12 días luego de la oviposición, pero las larvas no se alimentaron y eventualmente murieron. De manera similar, a 38,8 °C (93 °F) los huevos eclosionaron luego de 5,6 días, pero ninguna larva llegó al estado de pupa (Revynthi et al. 2022). En el sur de Florida, el pico de actividad de este picudo ha sido observado desde marzo hasta junio con bajas poblaciones desde septiembre hasta febrero.
Desarrollo de técnicas de manejo de plagas y monitoreo
Los programas de manejo integrado de plagas dirigidos al picudo del botón del hibisco contienen una combinación de prácticas culturales, sanitización, control químico y control biológico. La rotación de cultivos con especies no hospederas ha sido recomendada para interrumpir los ciclos de población (Bográn et al. 2003). La sanitización incluye la recolección y destrucción sistemática de todos los botones caídos al suelo. A pesar de que la sanitización es una labor de alta demanda de mano de obra, ha sido propuesta como una de las prácticas más eficientes en el manejo de esta plaga puesto que evita la reinfestación de las plantas con nuevos adultos (Bográn et al. 2003). Actualmente no existen insecticidas registrados específicamente para el control del picudo del botón del hibisco en Florida, pero los cultivadores pueden usar legalmente insecticidas que están registrados para su uso en viveros. La FDACS-DPI tiene una lista de insecticidas recomendados para el control de esta plaga. Las pruebas de eficacia de varios insecticidas registrados para picudos/coleópteros y otras plagas especificas en plantas ornamentales están actualmente en desarrollo. Hasta la fecha no existen reportes de enemigos naturales del picudo del botón del hibisco, pero en la actualidad se está estudiando el potencial uso de hongos y de nematodos entomopatógenos como agentes de control biológico.
Varias especies dentro del género Anthonomus son atraídas hacia un grupo de atrayentes comerciales que consisten en feromonas de agregación del macho y compuestos volátiles vegetales (Tumlinson et al. 1969; Eller et al. 1994; Innocenzi et al. 2001). Existen cuatro componentes de la feromona sintética de agregación del macho, también conocidos como Grandlures (I-IV). En la actualidad se está estudiando el uso de trampas de feromonas utilizadas ampliamente en otras especies de Anthonomus, para el caso del picudo del botón del hibisco. En Texas, las trampas de feromonas desarrolladas para el picudo del algodonero (A. grandis) fueron evaluadas, sin éxito, en la captura de adultos del picudo del botón del hibisco (Bográn et al. 2003). Sin embargo, los autores plantean que esto pudo haber ocurrido ante una ubicación temprana de las trampas de acuerdo con la temporada de aparición de los adultos. Las trampas pegajosas amarillas son las trampas más atractivas para varias especies de Anthonomus (Cross et al. 2006; Szendrei et al. 2011; Silva et al. 2018). Actualmente se adelantan pruebas de campo que estudian el poder atrayente de las feromonas del picudo del algodonero (A. grandis) y del picudo del chile (A. eugenii), y para poder identificar el mejor tipo de trampa para capturar los adultos del picudo del botón del hibisco. Es necesario un programa de manejo integrado de plagas que implemente las estrategias mencionadas anteriormente para regular las poblaciones de A. testaceosquamosus en Florida y disminuir el impacto económico causado por esta especie.
Referencias
Bográn CE, Helnz KM, Ludwlg S (2003) The bud weevil Anthonomus testaceosquamosus, a pest of tropical hibiscus. In: SNA Research Conference Entomology. pp 147–149
Capinera, J. L. (2002). Pepper weevil Anthonomus eugenii Cano (Insecta: Coleoptera: Curculionidae). Featured Creatures, University of Florida EENY-278
Clark WE, Burke HR, Jones RW, Anderson RS (2019) The North American Species of the Anthonomus squamosus Species-Group (Coleoptera: Curculionidae: Curculioninae: Anthonomini). Coleopt Bull 73:773. https://doi.org/10.1649/0010-065X-73.4.773
Cross JV., Hesketh H, Jay CN, et al (2006) Exploiting the aggregation pheromone of strawberry blossom weevil Anthonomus rubi Herbst (Coleoptera: Curculionidae): Part 1. Development of lure and trap. Crop Prot 25:144–154. https://doi.org/10.1016/j.cropro.2005.04.002
Eller FJ, Bartelt RJ, Shasha BS, et al (1994) Aggregation pheromone for the pepper weevil, Anthonomus eugenii cano (Coleoptera: Curculionidae): Identification and field activity. J Chem Ecol 20:1537–1555. https://doi.org/10.1007/BF02059879
Hunsberger A, Pena JE (1998) Biodynamics of Anthonomus macromalus (Coleoptera : Curculionidae ), a weevil pest of Barbados Cherry in Florida. Florida Entomol 334–338
Innocenzi PJ, Hall DR, Cross JV. (2001) Components of male aggregation pheromone of strawberry blossom weevil, Anthonomus rubi Herbst. (Coleoptera: Curculionidae). J Chem Ecol 27:1203–1218. https://doi.org/10.1023/A:1010320130073
Loiácono MS, Marvaldi AE, Lanteri AA (2003) Description of larva and new host plants for Anthonomus rubricosus Boheman (Coleoptera: Curculionidae) in Argentina. Entomol News 114:69–74
Mannion C, Hunsberger A, Gabel K, et al (2006) Hibiscus bud midge (Contarinia maculipennis)
Revynthi, A.M.; Velazquez Hernandez, Y.; Canon, M.A.; Greene, A.D.; Vargas, G.; Kendra, P.E.; Mannion, C.M. 2022. Biology of Anthonomus testaceosquamosus Linell, 1897 (Coleoptera: Curculionidae): A New Pest of Tropical Hibiscus. Insects. 13. https://doi.org/10.3390/insects13010013
Silva D, Salamanca J, Kyryczenko-Roth V, et al (2018) Comparison of trap types, placement, and colors for monitoring Anthonomus musculus (Coleoptera: Curculionidae) adults in highbush blueberries. J Insect Sci 18:. https://doi.org/10.1093/jisesa/iey005
Skelley PE, Osborne LS (2018) Pest Alert Anthonomus testaceosquamosus Linell, the hibiscus bud weevil, new in Florida. Gainesville
Szendrei Z, Averill A, Alborn H, Rodriguez-Saona C (2011) Identification and field evaluation of attractants for the cranberry weevil, Anthonomus musculus Say. J Chem Ecol 37:387–397. https://doi.org/10.1007/s10886-011-9938-z
Tumlinson JH, Hardee DD, Gueldner RC, et al (1969) Sex pheromones produced by male boll weevil: Isolation, identification, and synthesis. Science 166:1010–1012. https://doi.org/10.1126/science.166.3908.1010
United States Department of Agriculture U (2017) Market Value of Agricultural Products Sold Including Food Marketing Practices and Value-Added Products : 2017 and 2012 Census of Agriculture 2017. 275–302